The State of Microbiocenosis of the Large Intestine in Children against the Background of Systemic Therapy with an Antimycotic
Annotation
The study was aimed at evaluating the effect of a tablet antimycotic on the normal flora of the large intestine in the treatment of scalp microsporium in children. Materials and methods. The microbiota of the large intestine was studied using bacteriological analysis in 48 patients from rural areas, aged 3 three to 12 years, with microsporium of the scalp. The studies were conducted before the use of griseofulvin at a dose of 21–22 mg/kg per day for six weeks, on the tenth and twentieth days of therapy. It was found that by the 31.01 ± 2.85 day of treatment, a full clinical effect was observed, including the absence of fluorescence in the UFL and the eradication of the pathogen in the foci. Before treatment, the normal flora of the large intestine of rural children was dominated by a bifidus-dominant composition. By the twentieth day of treatment, the average concentrations of bifidobacteria had decreased to 106 CFU/g (a decrease of 40.0 %) (p ⩽ 0.05) and lactobacilli had decreased to 105 CFU/g (a decrease of 28.6 %) (p ⩽ 0.05), compared to the initial level. Conclusion. The study revealed a side effect of griseofulvin during long-term oral administration, which is expressed in a decrease in the concentration of the main families of normal flora in the microbial landscape of the large intestine of children without combining it with drugs that normalize the species composition of the intestinal microflora.
Unfortunately, the article is available only in Russian
Введение
Микроспория – заболевание из группы дерматофитий, сопровождающееся поражением гладкой кожи и её придатков, а также волосистой части головы. Она является наиболее распространённой патологией среди всех микозов у детей [Климко, 2017; Кубанов и др., 2021].
Показанием к системному назначению антимикотика являются микоз с поражением волосистой части головы или многоочаговое поражение гладкой кожи и пушковых волос. Для этого рекомендованы следующие лекарственные средства. Как альтернативные препараты: Тербинафин (В1) из группы аллиламинов в лечебной дозировке из расчета от массы тела в течение 4–8 недель; из группы азолов – Флуконазол (СII) по 6 мг/кг в сутки 6–8 недель или Итракрназол до 200 мг в сутки 6–8 недель. Но препаратом выбора в лечении детей является Гризеофульвин, с доказанностью (А1) назначаемый 6–8 недель до клинического выздоровления, подтвержденного отсутствием свечения в УФЛ и элиминацией патогенных грибов в очагах [Федеральные клинические…, 2016; Фомочкина, 2023]. Помимо фунгистатического действия, Гризеофульвин также обладает сосудорасширяющим, фотосенсибилизирующим, гепатотоксичным и выраженным иммуносупрессивным эффектами [Климко, 2017].
В составе кишечной микробиоты человека идентифицировано 2 172 вида микроорганизмов, разделённых на 12 таксономических типов, из которых 93,5 % принадлежали к Proteobacteria; Firmicutes; Bacteroidetes и Actinobacteria. Из них более трёхсот видов являются строго анаэробными, с наибольшей концентрацией бактерий в толстом кишечнике, где фирмикуты составляют более 60 % всего кишечного микробиома [Шендеров и др., 2016; Thursby et al., 2017; Vignesh et al., 2024]. Основными представителями семейств здоровой микробиоты кишечника являются Bifidobacteriaceae, Lactobacillaceae, Enterobacteriaceae, Bacteroidaceae, Clostridiaceae, Prevotellaceae, Eubacteriacea, Ruminococcaceae, а также археи [Tsubokawa et al., 2022].
У 70 % людей в кишечнике обнаруживаются Echerichiacoli и эукариоты рода Candida [Пахомовская и др., 2018].
Известно, что в микробном пейзаже кишечника в постнатальном периоде новорождённых детей доминируют филы Firmicutes, Protobacteria, Actinobacteria, к которым относят известные 60 видов бифидобактерий с меньшим количеством Bacteroidetes, но при последующей колонизации желудочно-кишечного тракта бактериями, поступающими с пищей извне, до 12 лет формируется нормофлора взрослых. При этом количество бифидобактерий в толстом кишечнике детей составляет 8–98 % с концентрацией 10 9 – 10 18 микробных тел в одном грамме содержимого [Сафина и др., 2021; Harmsen et al., 2000].
В настоящее время рядом ученых определены важнейшие функции бифидной микрофлоры. Она формирует кишечный барьер, защищая организм от колонизации кишечника патогенными микроорганизмами, поддерживая морфогенез слизистой кишечника. Стимулирует иммунную систему, экспрессируя макрофаги и лимфоциты за счет наличия мурамилпептида в бактериальной клеточной стенке. Способствуют метаболизму витаминов, крахмала, микро- и макроэлементов [Abdulgadir et al., 2000; Harmsen et al., 2000; Nassir et al., 2024; Sibanda et al., 2024].
Лактобактерии – грамположительные палочки, одни из главных составляющих нормофлоры, концентрация которых в кишечнике детей уже после одного года достигает
10 7–10 8 КОЕ/г, также выполняют целый ряд полезных функций. Выделяют вещества, обладающие бактерицидными свойствами (лизоцим, перекись водорода, бактериоцины). Участвуют в иммуногенезе, стимулируя выработку короткоцепочных жирных кислот, интерферонов и иммуноглобулинов. Кроме этого, бифидо- и лактобактерии обеспечивают гиполипидемический эффект путем деконъюгации солей желчных кислот, ассимиляции и преципитации холестерина, стимулируют пристеночное пищеварение. Способствуют восстановлению слизистой оболочки кишки, сохранению моторики кишечника и препятствуют заселению патогенных гнилостных, гноеродных и газообразующих микроорганизмов [Сафина и др., 2021; Мартынов и др., 2025; Mpountouridis et al., 2024; Olteanu et al., 2024].
Целый ряд экзогенных и эндогенных факторов может разрушать равновесие микробиоценоза кишечника. Воспалительные заболевания органов пищеварительной системы, сердечно-сосудистая патология, искусственное вскармливание, колонизация гельминтами и простейшими, приём антимикробных препаратов практически всегда приводят к дисбактериозу, побочным симптомокомплексам и возможной резистентности к терапии [Ливзман и др., 2025; Степанов и др. 2025; Pant et al., 2023]. Современные исследования показали, что одним из наиболее значимых и распространённых нарушений микробиоценоза толстой кишки является недостаточность бифидобактерий, которая может усугубляться и длительностью лекарственного воздействия на микрофлору [Al Bander et al., 2020; He Bao-Lin et al., 2023; Bajaj et al., 2025].
Определение бифидо- и лактобактерий считается наиболее информативным критерием диагностики дисбактериоза кишечника.
Может ли влиять на микрофлору кишечника детей длительное применение гризеофульвина в системной терапии микроспории с поражением волос, создавая эффект накопления, подлежит исследованию.
Цель исследования
Оценить влияние таблетированного антимикотика при пероральном применении на нормофлору толстого кишечника у сельских детей при длительном лечении микроспории волосистой части головы.
Объекты и методы исследования
Было проведено простое проспективное клиническое исследование. Объём наблюдений составил 68 человек. Из них: 48 пациентов (39 мальчиков – 62,5 %, 18 девочек – 31,5 %) из сельской местности региона, соответствующих критериям включения в возрасте от 3 до 12 лет (средний возраст 6,8 ± 1,9 года), находившихся на стационарном лечении в микологическом отделении БУЗ Орловской области «Орловский кожно-венерологический диспансер» с диагнозом – микроспория волосистой части головы. Также в качестве группы сравнения обследовано 20 детей, жителей областного центра, в гастроэнтерологическом кабинете БУЗ Орловской области «Детская поликлиника № 1».
Критериями включения в исследовательскую группу были: больные дети с диагнозом микроспории волосистой части головы (В35.0 по классификации МКБ), подтверждённым свечением очагов в люминесцентной лампе Вуда и идентификацией возбудителя культуральным методом, у которых отсутствовали противопоказания к лечению данным антимикотиком, инфекционные состояния, требующие приёма антибактериальных средств, любая патология печени и ЖКТ; наличие аллергии к лекарствам; информированное добровольное согласие родителей на проведение данного клинического, бактериологического обследования и лечения.
Согласно протоколу исследования, перед началом лечения и на 10-й и 20-й дни терапии исследование микробиоты кишечника проводилось на базе гастроэнтерологического кабинета и микробиологической лаборатории детской поликлиники № 1 г. Орла. В клинической и бактериологической лабораториях диспансера проводились стандартные и биохимические исследования два раза в течение цикла лечения. Терапия микроспории проводилась с поэтапным уменьшения дозы гризеофульвина. Критериями этому служили: эррадикация мицелия грибов из очагов воспаления и отсутствие свечения поражённых волос в лучах лампы Вуда. Сопутствующая наружная терапия включала противогрибковые средства в виде растворов и мазей, еженедельно проводилась эпиляция волос в очагах [Федеральные клинические…, 2016].
Лабораторные исследования фекальной микробиоты толстого кишечника производились методом бактериологического анализа. В соответствии с отраслевым стандартом «Дисбактериоз кишечника. Протокол ведения больных» проведена оценка результатов 164 копрологических проб, из которых – 144 пробы, полученные у 48 больных сельских детей, и 20 проб – у здоровых детей, проживающих в областном центре, в качестве контроля сравнения перед началом лечения. Утренний образец стула (не менее 5 г) направлялся в бактериологическую лабораторию в течение 1–2-х часов в стерильных контейнерах. После посева на плотных и жидких питательных средах, Сабуро, Левина, кровяной и желточно-солевой агары, также на среду aгар MRS (de Man, Rogosa и Sharp agar) для определения роста бифидо- и лактобактерий при инкубации от 1 до 6 суток осуществлялся подсчёт выросших колоний, выраженных в колониеобразующих единицах при десятикратном разведении [Минздрав России, 2003].
Оценку микробиоценоза проводили методом количественного определения видов микроорганизмов, входящих в состав, с последующим изучением связей динамики изменения с длительностью применения и курсовой дозой гризеофульвина.
Для статистического анализа использовали пакет статистических программ SPSS 17.0. Достоверность различий средних величин определялась на основании непарного критерия Стьюдента (t) и Т-критерия Уилкоксона, при (p ⩽ 0,05) различия считались статистически достоверными при параметрическом распределении признаков. Для выявления средней арифметической признака при изучении количественной характеристики микрофлоры применяли выборочную среднюю 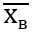
Результаты и их обсуждение
При анализе клинических проявлений было установлено, что у 40 человек (83 %) на коже волосистой части головы имелось от 2 до 8 очагов поражения размером от 1 до 4 см, и только у 8 детей диагностировалось по одному крупному очагу, независимо от пола и возраста. Время с момента появления симптомов до обращения к врачам – от 5 до 13 дней, что может говорить о влиянии социального быта на клинику заболевания. Волосы в очагах были обломаны (как бы подстрижены) на уровне от двух до восьми миллиметров. Очаги имели четкие границы, слабовыраженный характер воспаления с муковидным шелушением на поверхности. Сочетанное поражение волосистой части и гладкой кожи наблюдалось в 33,3 % случаев.
Анализ регресса симптомов показал следующее. Элиминация грибов рода Microsporum происходила на 19 ± 4,16 день в очагах на волосистой части головы и на 14 ± 1,56 день в очагах на гладкой коже. Исчезновение свечения поражённых волос наблюдалось к 21,01 ± 1,74 дню. Полное клиническое выздоровление регистрировалось в среднем на 31,01 ± 2,85 день лечения. При последующих контрольных обследованиях грибов при отрастании волос в очагах не отмечалось.
В процессе терапии достоверно выраженных изменений в биохимических показателях и лейкоцитарной формуле крови у детей не наблюдалось.
Полученные данные микробной составляющей кишечника показали её разнообразный состав. Частота встречаемости микроорганизмов в микробиоте кишечника была следующей. До лечения в микробиоте детей, проживающих в сельской местности, преобладал бифидодоминантный состав микрофлоры толстого кишечника, который не отличался от микробиоценоза городских детей. У всех 48 пациентов (100 %) были определены микроорганизмы – Bifidobacteriumspp., Lactobacillusspp., Enterobacteriaceae, Echerichiacoli в концентрациях, определяющих норму, которые сохранялись на протяжении всего цикла лечения. Также у всех высевались Enterococcusspp., которые на десятый день были только у 20 детей (41,7 %) (p ⩽ 0,05) и исчезли к 20-му дню.
Из условно патогенных энтеробактерий были выделены микроорганизмы у одного пациента (2,1 %) – Klebsiella pneumonia в концентрации 10 5 КОЕ/г и Proteus vulgaris. У двух пациентов (4,2 %) выделены Klebsiella oxytoca в концентрации > 105 КОЕ/г, причём у одного из них данный микроорганизм определялся и после 10-го дня наблюдений в количестве 10 4 КОЕ/г. У одного ребёнка обнаружены анаэробные сульфитредуцирующие Clostridium perfringens – 10 5 КОЕ/г. Также перед началом лечения в микробном пейзаже толстого кишечника у мальчика присутствовали Enterobacter cloacae и Citrobacter Kloseri в концентрациях 10 6 КОЕ/г и у одной пациентки – гемолитические Escherichia coli в концентрации 10 7 КОЕ/г. У 38 больных детей (79,2 %) обнаружены лактозонегативные эшерихии, на 10-й день определялись только у (25,0 %) 12 детей (p = 0,01). Стафилококки в общем количестве высевались у 29 человек (60,4 %), а на 10-й день – только у 8 пациентов (16,7 %) (p = 0,001), Staphylococcusaureus в кале не определялся. У четырёх детей (8,3 %) до лечения присутствовали грибы рода Candida в концентрации 10 5 – 10 6 КОЕ/г. В последующих копрологических пробах происходило исчезновение данной микрофлоры с десятого по двадцатый дни наблюдений.
В результате проведённых исследований установлены статистически значимые качественные сдвиги микрофлоры ЖКТ у сельских детей на фоне терапии.
Наряду с качественными изменениями видового состава нормофлоры толстого кишечника наблюдаются и количественные изменения. Было выявлено, что если до лечения содержание Bifidobacteriumspp. в исследуемых копропробах было в норме (рисунок 1), то к десятому дню лечения их концентрация уменьшилась в среднем на 30 %, а к двадцатому дню – ещё на 10 % до 1,0*106 КОЕ/г (p ⩽ 0,05), по сравнению с исходным уровнем. У 6,3 % (3 человека) – 10 4; 62,5 % (30 человек) – 10 5; 16,7 % (8 человек) – 10 6; 10,4 % (5 человек) – 10 7; 4,2 % (2 человека) – 10 9 КОЕ/г.
Аналогичная динамика наблюдается с Lactobacteriumspp. (рисунок 2), концентрация которых уже на 10 день лечения уменьшилась на 28 % по сравнению с исходным уровнем
в среднем до 1,0*10 5 КОЕ/г (p ⩽ 0,05) с сохранением этой концентрации до двадцатого
дня наблюдений. Это говорит о выраженном количественном изменении состава
основной микрофлоры кишечника у детей на фоне длительного применения
гризеофульвина.
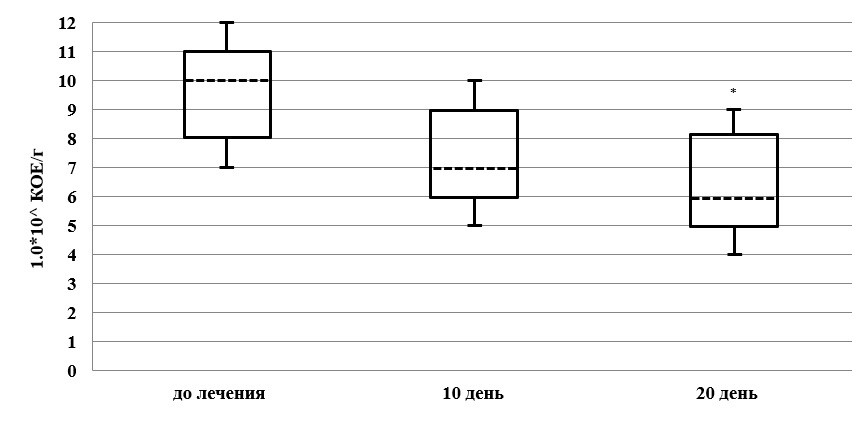
Рис. 1. Динамика изменения концентрации Bifidobacteriumspp у пациентов в ходе лечения (M ± m)
Fig. 1. Dynamics of changes in the concentration of Bifidobacterium spp in patients during treatment (M ± m)
Примечание к рис. 1: КОЕ от 0 до 10 12/мл; * – (p ⩽ 0,05) достоверность отличий по отношению к показателям до лечения; [T] – максимальный показатель; [L] – минимальный показатель; [---] – средняя величина.
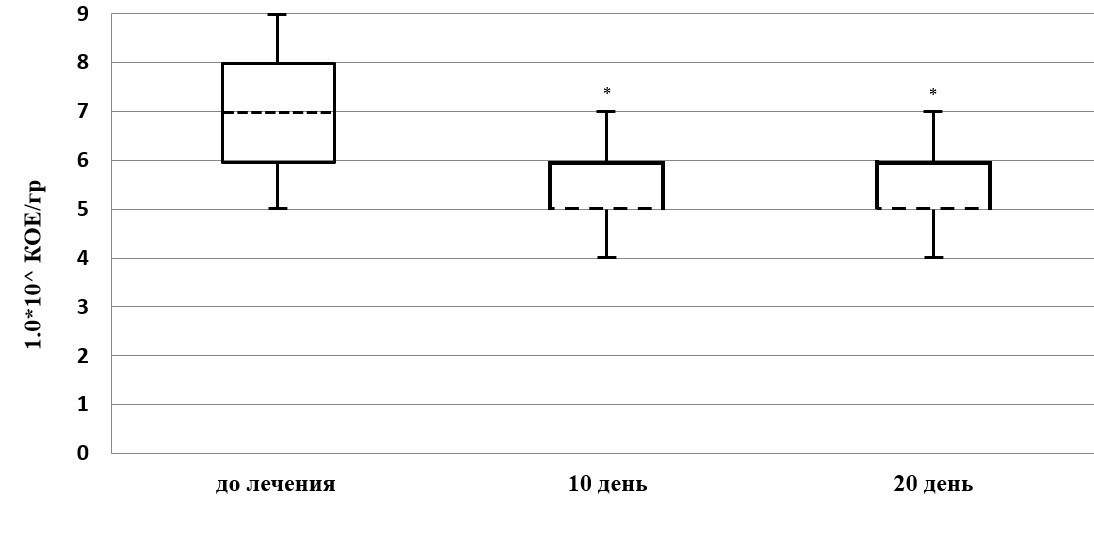
Рис. 2. Динамика изменения концентрации Lactobacteriumspp у пациентов в ходе лечения (M ± m)
Fig. 2. Dynamics of changes in the concentration of Lactobacterium spp in patients during treatment (M ± m)
Примечание к Рис. 2: КОЕ от 0 до 109/мл; * – (p ⩽ 0,05) достоверность отличий по отношению к показателям до лечения; [T] – максимальный показатель; [L] – минимальный показатель; [---] – средняя величина.
Таким образом, видим побочное влияние таблетированного препарата на всю микрофлору кишечника детей.
Обсуждение
В нашем исследовании показано, что данный системный антимикотик проявляет выраженное терапевтическое действие на грибы Microsporum, это подтверждается отсутствием в дальнейшем рецидивов заболевания.
Гризеофульвин относится к группе гризанов, являясь хлорсодержащим антибиотиком, его молекула сходна с молекулой пенициллина. Данное вещество синтезируется плесневым грибком рода Penicillinum nigricans (griseofulvinum), обнаружено в культуре гриба в 1938 году [Marto et al., 2016]. Griseofulvinum имеет химическое название – (1'S-транс)-7-Хлор-2',
4,6-триметокси-6'-метилспиро [бензофуран-2(3H),1'-[2] циклогексен]-3,4'-дион [Enna, 2008].
Этот препарат обладает фунгистатическим действием преимущественно на грибы рода дерматофитов (Microsporum, Trichophyton и Epidermophyton). Это его действие имеет два направления. Во-первых, происходит нарушение синтеза ДНК. В результате этого прекращается спорообразование и рост грибов. Во-вторых, в результате нарушения синтеза белка происходит разрушение клеточной стенки. С учетом фармакокинетики при пероральном применении его доступность колеблется от 25 до 70 % за счёт плохой растворимости в воде, а пиковая концентрация в плазме крови наступает через 4 часа [Климко, 2017]. Наиболее высокие дозы концентрации наблюдаются в роговом слое кожи и в волосах за счёт проникновения в клетки-предшественники кератина. Он также концентрируется в ногтях, печени, мышцах и жировой ткани [Enna, 2008].
Утилизация его происходит посредством окислительного демителирования при связывании с глюкуроновой кислотой в печени до 6-десметилгризеофульвина. Период полураспада гризеофульвина составляет от 9 до 12 часов, и в течение 5 часов тридцать процентов его выводится с калом [Enna, 2008].
Согласно клиническим рекомендациям при поражении волосистой части головы Microsporum для достижения стойкого клинического эффекта в целях увеличения биодоступности препарата и уменьшения побочных дозозависимых негативных действий гризеофульвина его назначают в течение 2–3 недель во время или сразу после еды в дозе
21–22 мг/кг веса ребенка ежедневно три раза в сутки до полной эррадикации возбудителя в очагах и отсутствия свечения волос лучах лампы Вуда. Далее кратность приема антимикотика такова – назначается через день ещё две недели до второго отрицательного анализа. Далее – ещё две недели через 48 часов до следующего позитивного результата обследования [Яковлев, 2019; Медведева и др., 2020].
Полученные нами результаты показали, что при длительном использовании гризеофульвина при микроспории с поражением волос у детей происходит исчезновение условно-патогенных микроорганизмов. Отсутствовали в посевах на десятый день лечения: Klebsiella pneumonia и Proteus vulgaris, также Enterobacter cloacae и Citrobacter Kloseri, гемолитические Escherichia coli, грибы рода Candida (p = 0,0). К 20-му дню терапии в фекалиях детей не обнаруживались Сульфитредуцирующие Clostridium perfringens, Klebsiella oxytoca, лактозонегативные Escherichia coli (p = 0,0). И если облигатная микрофлора кишечника сохраняется, то крайне отрицательным моментом является токсическое действие лекарства на доминантную главную и сопутствующую флору кишечника детей, снижая её защитные свойства, если учесть, что бактерии семейства Enterobacter spp. обладают некоторыми факторами патогенности, такими, как продукция эндотоксинов и инвазивная способность с выживаемостью внутри фагоцитов [Кокорев и др., 2025].
В нашем случае, несмотря на применение таблетированного гризеофульвина во время еды с 1 чайной ложкой растительного масла для его лучшей всасываемости и ослабления токсичности, наблюдается значительное уменьшение количества симбиотических бактерий, высеваемость которых к 20-му дню лечения составляла в среднем рода Bifidobacterium spp. – 1,0*106 КОЕ/г и рода Lactobacteriumspp – 1,0*105 КОЕ/г. Такой дисбаланс нормофлоры кишечника может влиять на пристеночное пищеварение и, как следствие, всасывание из химуса водорастворимых лекарственных соединений и жирорастворимого витамина К. Данный витамин (менахинон), участвующий в формировании костной ткани и синтезе 16 типов белков, обладает противовоспалительным действием, поэтому необходим детскому организму [Костюченко и др., 2018].
В Российской Федерации для перорального приема гризеофульвин представлен в виде таблеток и суспензий по 0,125 г и 0,5 г с плохой растворимостью в воде, что уменьшает его биодоступность [Климко, 2017], это вынуждает врачей увеличивать терапевтическую дозу препарата и время лечения микроспории.
Один из подходов, направленных на снижение системной токсичности гризеофульвина, – необходимость его комбинации с препаратами, нормализующими микробиоту кишечника, в совместном решении этого вопроса с гастроэнтерологами.
Для нормализации микрофлоры преимущественными средствами являются пробиотики, содержащие живые бактериальные пробиотические клетки, разделённые на нутрибиотики и фармабиотики. Наиболее перспективные из них: мультипробиотик – Лактобаланс; Бифиформ; Пробиель проэнзим; Линекс форте; БАК-СЕПТ форте; Бифидумбактерин ВВ-12 и Лактобактер LGG [Андреев, 2022; LeBegue, 2020; Higuchi et al., 2024; Marole et al., 2024; Poeta et al., 2024; Sibanda et al., 2024], тем более что у детей эффективность пробиотиков выше, чем у взрослых [Мескина, 2025].
Другой подход – совершенствование применения различных носителей лекарственной субстанции. Для адресной доставки водонерастворимых антимикотиков предложены контейнеры-носители на основе липосом, эмульсий, везикул, различных типов нано- и микрочастиц [Marto et al., 2016; Zhongvi et al., 2020; Gusliakova et al., 2021; Wei Du et al., 2021]. Применение таких форм обеспечивает увеличение глубины проникновения и эффективности при концентрации антимикотика в целевой области, что улучшает биодоступность, а также продлевает терапевтический эффект и одновременно сокращает суммарную терапевтическую дозу препарата [Singh et al., 2024]. Но эти исследования касались только наружного использования лекарственных средств.
Выводы
Полученные результаты негативного влияния длительного приёма гризеофульвина на нормофлору толстого кишечника у детей представляют интерес для практической медицины и фармацевтики. Исследования показали, что проблема коррекции кишечной микрофлоры в данном случае является значимой и её нельзя недооценивать. Для поддержания нормальной микрофлоры кишечника и предупреждения таксономических изменений при терапии необходимы эу-, пре- и пробиотики и дальнейшие исследования, направленные на повышение биодоступности и безопасности пероральных антимикотиков.





Reference lists
Andreev V.A., Stetsyuk O.U., Andreeva I.V. 2022. Probiotics: An Unresolved Problem. Clinical Microbiology and Chemotherapy. 24(4): 345–360 (in Russian). doi: 10.36488/cmac2022.4.345-360
Klimko N.N. 2017. Mycoses: Diagnosis and Treatment. A Guide for Doctors. 3rd edition. Moscow: Pharmtek, 272 p. (in Russian).
Kostyuchenko L.A., Kharitonova N.S., Vdovin V.M. 2018. The Effectiveness of Using a Vitamin Complex: Vitamin D and Vitamin K (Literature Review). Bulletin of Medical Science. 11(3): 33–40 (in Russian).
Kokorev D.A., Strazhina E.A., Kabanova N.P., Yankovaya Z.A., Konstantinov D.Y., Lyamin A.V. 2025. Features of Pathogenicity Factors of Enterobacteriaceae Family Members Involved in the Development of Necrotizing Enterocolitis. Medical Council. (19): 154–165 (in Russian). https://doi.org/10.21518/ms2025-348
Kubanov A.A., Bogdanova E.V. 2021. The Result of the Activities of Medical Organizations Providing Medical Care in the Field of Dermatovenerology in 2020: Work in a Pandemic: Bulletin of Dermatology and Venereology. 97(4): 8–33 (in Russian). https://doi.org/10.25208/vdv1261
Lagutin M.B. 2025. Visual Mathematical Statistics. Binom: Knowledge Laboratory. 472 p. (in Russian).
Livzman M.A., Borodin D.S., Abdulkhanov S.R. 2025. Constipation, Intestinal Microbiota and Comorbid Pathology: The Search for an Optimal Approach to Patient Management. Breast Cancer. MRJ. Medical review. 9(9): 596–605 (in Russian). doi: 10.32364/2587-6821-2025-9-9-9
Martynov N.S., Ponezheva Zh.B., Kulikova N.G., Bityunina L.A., Lazareva E.N., Usenko D.V., Vdovina E. 2025. Systemic Inflammation and Intestinal Microbiocenosis in COVID-19: The Role of Macrophage Inflammatory Proteins in the Pathogenesis of the Disease. MRJ. Medical review. 9(5): 259–265 (in Russian). doi: 10.32364/2587-2025-9-5-1
Medvedeva T.V., Leina L.M., Chilina G.A., Petunova Ya.G., Pchelin I.M. 2020. Microsporia: Current Views on the Problem (Description of Clinical Cases and Literature Review). Problems of Medical Mycology. (2): 12–21 (in Russian). doi: 10.24412/1999-6780-20202-12-21
Meskina E.R. 2025. Treatment of Acute Infectious Diarrhea in Children: Current Trends and Open Issues. RMJ. Mother and Child. 8(3): 263–270 (in Russian). doi: 10.32364/2618-8430-2025-8-3-12
Russian Ministry of Health. 2003. "Protocol for the Management of Patients. Intestinal Dysbiosis" / OST 91500.11.0004-2003. Order of the Ministry of Health of the Russian Federation No. 231. 06/09/2003. (in Russian) (Electronic Resource) URL: https://www.base,garant.ru (access date 07.10. 2025)
Pakhomovskaya N.L., Venedittova M.M. 2018. Healthy Colonization in Children – Strong Immunity. Meditsinskiy sovet. 17: 199–205 (in Russian). https://doi.org/10.21518/2079-701X-2018-17-199-205
Ruzhentsova T.A., Garbuzov A.A., Bayrakova A.L. 2025. The Effect of Probiotic Therapy on the Clinical Manifestations of Neuropsychiatric Disorders in Patients with Dysbiotic Changes. RMJ. Medical Review. (5): 2 2–28 (in Russian). doi: 10.32364/2225-2282-2025-5-5
Safina D.D., Abdulkhakov S.R., Amirov N.B. 2021. Intestinal Microbiota and its Significance for Human Health. Bulletin of Modern Clinical Medicine. 14(5): 81–94 (in Russian). doi: 10.20969/VSKM.2021.14(5).81-94
Stepanov M.S., Karpunina N.S., Spasenkov G.N. 2025 The Microbial Composition of the Colon and the Levels of Certain Pro-Inflammatory Serum Molecules in the Long-Term Period in Patients with Myocardial Infarction. RMJ; Medical Review. 9(5): 275–280 (in Russian). doi: 10. 32364/2587-6821-2025-9-5-3
Fomochkina Е.А. 2023. Microsporia (Ringworm) (in Russian). (Electronic Resource) URL: https://probolezny.ru/mikrosporiya / (access date 04.15.2025)
Federal Clinical Guidelines. Dermatovenerology. 2016. Skin Diseases. Sexually Transmitted Infections (2016). Kubanova A.A. (Edit.). Moscow: Delovoy Express, 768 p. (in Russian).
Shenderov B.A., Golubev V.L., Danilov A.V., Prishchepa A.V. 2016. Human Intestinal Microbiota and Neurodegenerative Diseases. Poliklinika. 1–1: 7−13 (in Russian).
Yakovlev A.B. 2019. Systemic Therapy of Mycoses of Hairy Skin Areas: The Possibilities of Adjuvant Drugs. Effective Pharmacotherapy. 15(11): 6–10 (in Russian). doi: 10.33978/2307-3586-2019-15-11-6-10
Abdulgadir A., Engers J., Al-Sadi. 2023. Role of Bifidobacterium in Modulating the Intestinal Epithelial Tight Junction Barrier: Current Knowledge and Perspectives. Curr Dev Nutrition. Oct 30; 7(12); 102026. doi: 10.1016/j.cdnut.2023.102026
Al Bander Z., Nitert M.D., Mousa A., Naderpoor N. 2020. The Gut Microbiota and Inflammation: An Overview. International Journal Environmental Research. 17(20): 7618. doi: 10.3390/ijerph17207618
Bajaj P., Sharma M. 2025. Chrononutrition and Gut Health: Exploring the Relationship Between Meal Timing and the Gut Microbiome. Curr Nutrition Rep. 2025 Jun 9; 14(1): 79. doi: 10.1007/s13668-025-00670-z
Enna S.J., Bylund D.B. xPharm: The Comprehensive Pharmacology Reference. 2008. (Electronicresource) URL:https://www.sciencedirect.com/referencework/9780080552323/xpharm-the-comprehensive-pharmacology-reference (access date 07.15. 2025)
Gusliakova O., Verkhovskii R., Abalymov A., Lengert E., Kozlova A., Atkin V., Nechaeva O., Morrison A., Tuchin V., Svenskaya Y. 2021. Transdermal Platform for the Delivery of the Antifungal Drug Naftifine Hydrochloride Based on Porous Vaterite Particles. Materials Science and Engineering: 119 p: 111428. doi: 10.1016/j.msec.2020.111428
Harmsen H.J.M., Wldeboer–Veloo А.С.М., Raangs G.C., Wagendorp А.А., Klijn N., Bindels J.G., Welling G.W. 2000. Analysis of Intestinal Flora Development in Breast–Fed and Formula–Fed Infants by using Molecular Identification and Detection Methods. Journal of Pediatric Gastroenterology and Nutrition. 30: 61–70. doi: 10.1097/00005176-200001000-00019
He Bao-Lin., Xiong Y., Hu Ten-Gen., Zong Min-Hua., Wu H. 2023. Bifidobacterium spp. as Functional Foods: A Review of Current Status, Challenges, and Strategies. Clinical Reviews in Food Scinsce and Nutrition. 63. (26): 8048–8065. doi: 10.1080/10408398.2022.2054934
Higuchi T., Furuichi M., Maeda N. Tsugawa T., Ito K. 2024. Effects of Probiotics in Children with Acute Gastroenteritis: A Systematic Review and Meta-Analysis Focusing on Probiotics Utilized in Japan. Journal Infection Chemother. 30(4): 337–342. doi: 10.1016/j.jiac.2023.11.005
LeBegue C.E., Love B.L., Watt M.D. 2020. Microbes as Drugs: The Potential of Pharmabiotics. Pharmacotherapy. 44(2): 102–106. doi: 10.1002/phar. 2357
Marole T., Sinbanda T., Buys E. 2024. Assessing Probiotic Viability in Mixed Species Yogurt Using a Novel Propidium Monoazide (PMAxx)-Quantitative PCR Method. Front Microbiology. Feb. 8(15): 1325268. doi: 10.3389/fmicb.2024/1325268.eCollection2024
Marto J., Vitor C., Guerreiro A., Severina C., Eleut´erio C., Ascenso A., Simo˜es S. 2016. Ethosomes for Enhanced Skin Delivery of Griseofulvin. Colloids end Surfaces B: Biointerfaces. 146: 616−623. https://doi.org/10.1016/j.colsurfb.2016.07.021
Mpountouridis A., Tsigalou C., Bezirtzoglou I., Bezirtzoglou E., Stavropoulou E. 2024. Gut Microbiome in Non-Alcoholic Fatty Liver Disease. Front Gastroenterol. (3): 1534431. doi: 10.3389/fgstr.2024.1534431
Nassir M., Ramli M., Ghazali M., Jaffer M., Hamid H., Mehat M., Hein Z. 2024. The Microbiota-Gut-Brain Axis: Key Mechanisms Driving Glymphopathy and Cerebral Small Vessel Disease. Life (Basel). Dec 24; 15(1): 3. doi: 10.3390/life15010003
Olteanu G., Ciucă-Pană M-A., Busnatu Ș., Luplisa D., Neacsu S., Mititelu M., Musus A., Lonita-Mindracan C-B., Boroghina S. 2024. Unraveling the Microbiome-Human Body Axis: A Comprehensive Examination of Therapeutic Strategies, Interactions and Implications. Int J Mol Sci. 25(10): 5561. doi: 10.3390/ijms25105561
Pant A., Maiti T., Mabajan D., Das B. 2023. Human gut Microbiota and Metabolism. Review. Microb Ecologi. 86(1): 97–111. doi: 10. 1007/s00248-022-02081-x
Poeta M., Del Bene M., Lo Vecchio A., Guarino A. 2024. Acute Infectious Diarrhea. Adv Exp Med Biol. 2024; 1449: 143–156. doi: 10.1007/978-3-031-58572-2_9
Sibanda T., Marole T., Thomashoff U., Thantsha M. 2024. Bifidobacterium Species Viability in Dairy-Based Probiotic Foods: Challenges and Innovative Approaches for Accurate Viability Determination and Monitoring of Probiotic Functionality. doi: 10.3389/fmicb.2024.1327010
Singh S., Patil V.M., Paliwal S.K., Masand N. 2024. Nanotechnology-based Drug Delivery of Topical Antifungal Agents. Pharmaceutical Nanotechnology. 12(3): 185–196. doi: 10.2174/2211738511666230818125031
Thursby E., Juge N. 2017. Introduction to the Human Gut Microbiota. Biochemical Journal. 474(11): 1823–1836. doi:10.1042/BCJ20160510
Tsubokawa M., Nishimura M., Mikami T., Ishida M., Hisada T., Tamada Y. 2022. Association of Gut Microbial Genera with Heart Rate Variability in the General Japanese Population: The Iwaki Cross-Sectional Research Study. Metabolites. 12(8): 730. doi: 10.3390/METABO12080730
Vignesh S.D., Vijayakumar T.M., Nandimandalam S.S. 2024. Impact of Food Intake and Slip Disturbances on Gut Microbiota. Reviw. Cureus. 16(10): e70846. doi: 10.7759/cureus.70846
Wei D., Yiru G., Li L., Sixiang S., Chen D. 2021. Striking Back against Fungal Infections: The Utilization of Nanosystems for Antufungal Strategies. International Journal Molecular Scientific. 22(18): 10104. doi: 3390/ijms221810104
Zhongvi M., Xiaoyou W., Chong L. 2020. Snrategies of Drug Delivery for Deep Fungal. Journal Farm Nanotechnologi. 8(5): 372–390. doi: 10.2174/2211738508666200910101923