Volume Fraction of Myocardial Interstitial Collagen in Patients with Stable Angina: Relationship with the State of the Coronary Bed and Global Longitudinal Deformation of the Left Ventricle
Annotation
The aim of the study was to evaluate the volume fraction of interstitial myocardial collagen in patients with stable angina pectoris depending on the state of the coronary bed and to analyze the relationship with the index of global longitudinal deformation of the left ventricle. The medical examination included 63 men with coronary artery disease: stable angina pectoris and preserved systolic function of the left ventricle (left ventricular ejection fraction greater than 50 % (Simpson's method)). At the time of the study, all patients had a sinus rhythm of the heart. Coronary angiography was performed according to the standard procedure. The index of global longitudinal deformation of the left ventricle was evaluated using speckle tracking technology in echocardiography. Based on the left ventricular myocardial mass index, the total voltage of QRS complexes in twelve standard electrocardiography leads, and the patient's height index, the volume fraction of interstitial collagen of the left ventricular myocardium was calculated. It was found that in patients with coronary artery disease: stable angina pectoris and preserved systolic function of the left ventricle, the degree of interstitial fibrosis of the left ventricle, estimated by the volume fraction of interstitial myocardial collagen, depends on the degree of coronary artery stenosis. In the group of patients with moderate atherosclerotic coronary artery disease (stenosis 21–70 %), a direct statistically significant moderate correlation between these indicators was established (r = 0.56, p = 0.039), while in the group of patients with severe coronary artery disease (stenosis ≥71 %), an even closer statistically significant correlation was revealed (r = 0.63, p = 0.031). With the progression of the atherosclerotic process in the coronary arteries, the degree of fibrosis of the left ventricular myocardium increases, which is associated with increased impairment of the global longitudinal systolic deformation of the left ventricle.
Keywords: stable exertional angina, volume fraction of interstitial collagen of the left ventricular myocardium, global longitudinal deformity of the left ventricle, coronary angiography, coronary artery stenosis
Unfortunately, the article is available only in Russian
Введение
Распространенность ишемической болезни сердца (ИБС) и ее осложнений, несмотря на некоторое снижение смертности от сердечно-сосудистых заболеваний в последние годы, остается высокой. Самой частой формой ИБС в популяции является стенокардия, причем с возрастом частота ее встречаемости увеличивается [Усачева и др., 2021; Бойцов, 2022].
В последние годы при изучении патофизиологических процессов ремоделирования миокарда вектор интересов сместился с изучения кардиомиоцитов на исследование внеклеточного матрикса, что инициировало активное проведение научных изысканий в этом направлении. Показано, что в перестройке внеклеточного матрикса центральным звеном является нарушение баланса обмена коллагена. Причем для хронических форм ИБС более характерен диффузный фиброз, который формируется в интерстициальном или периваскулярном пространстве миокарда, потерей количества функционирующих клеток миокарда это не сопровождается, но все же оказывает на них негативное воздействие [Гордеева и др., 2022; Schimmel et al., 2022]. Установлено, что фиброзирование внеклеточного матрикса миокарда может изменять контрактильность и биофизические свойства миокарда, которые можно оценить различными методами инструментальной диагностики, не прибегая к инвазивным методикам [Тарасова и др., 2023; Пономарева, Смирнова, 2024; Fan et al., 2020].
Представляет интерес уточнение степени выраженности фиброзных изменений у пациентов с ИБС в зависимости от состояния коронарного русла и выявление возможных статистически значимых связей с показателями инструментальных методов обследования. В связи с этим целью исследования стала оценка объемной фракции интерстициального коллагена миокарда у пациентов со стабильной стенокардией напряжения в зависимости от состояния коронарного русла и изучение связи с показателем глобальной продольной деформации левого желудочка.
Материалы и методы
На базе 2 кардиологического отделения ФГБУ «Клиническая больница № 1» УДП РФ обследовано 63 пациента-мужчины с ишемической болезнью сердца: стабильной стенокардией напряжения и сохраненной систолической функцией левого желудочка (фракция выброса левого желудочка (ФВ ЛЖ) более 50 % (метод Симпсона)). На момент исследования у всех пациентов регистрировался синусовый ритм сердца. Критериями исключения из исследования были возраст старше 65 лет, инфаркт миокарда в анамнезе, нестабильная стенокардия давностью менее 6 месяцев, кардиохирургическое лечение в анамнезе, врожденные пороки сердца, степень стенозирования коронарных артерий менее 20 % по данным коронарографии, злокачественные новообразования, острые инфекционные и воспалительные процессы и/или хронические воспалительные процессы в стадии обострения, эндокринная патология (в стадии декомпенсаци, прием глюкокортикоидов), заболевания почек с нарушением их функции (снижение скорости клубочковой фильтрации менее 60 мл/мин / 1,73 м2); заболевания печени с нарушением ее функций (повышение уровней печеночных ферментов в 3 раза и более), аутоиммунные заболевания, системные заболевания соединительной ткани.
Диагноз устанавливался в соответствии с клиническими рекомендациями «Стабильная ишемическая болезнь сердца» (2024 год) Министерства здравоохранения Российской Федерации и формулировался по Международной классификации болезней (МКБ-10, Женева, 1992 год). Функциональный класс стенокардии устанавливался по классификации Канадского кардиологического общества (1976 год). Диагноз ХСН устанавливался в соответствии с клиническими рекомендациями «Хроническая сердечная недостаточность» (2024 год) Министерства здравоохранения Российской Федерации. С использованием классификации Нью-Йоркской ассоциации кардиологов (New York Heart Association) (1994 год) оценивали тяжесть хронической сердечной недостаточности.
Все пациенты давали информированное добровольное согласие на включение в исследование.
Исследование было выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинской Декларации, протокол исследования был одобрен Этическим комитетом.
Коронарография проводилась на установке Siemens Artis Zee (Германия) по стандартной методике [Абдрахманова и др., 2020; Миронова и др., 2023]. За 1 день до коронарографии проводилась эхокардиография (ЭХОКГ) по стандартной методике на аппарате Philips EPIQ 7 (США), с использованием технологии спекл-трекинг оценивался показатель глобальной продольной деформации левого желудочка (GLS) [Мухаметгареева и др., 2020].
Расчёт объемной фракции интерстициального коллагена в миокарде (ОФИК) производился по формуле, разработанной Shirani J. и соавторами, с использованием показателя массы миокарда левого желудочка (расчёт по формуле Penn Convention по данным ЭХОКГ), показателя общего вольтажа комплексов QRS в двенадцати стандартных отведениях (по данным ЭКГ) и показателя роста пациента:
где ОФИК – объемная фракция интерстициального коллагена, ММЛЖ – масса миокарда ЛЖ.
Референсный диапазон ОФИК составил 2–6 % [Shirani et al., 1992].
Программа STATISTICA 12.0. применялась для статистической обработки данных. В виде значения медианы (Ме) и интерквартильного размаха (от 5 процентиля до 95 процентиля) в результатах исследования приводились полученные в исследовании показатели. Проверка статистических гипотез при сравнении числовых данных двух несвязанных групп производилась с использованием критерия Манна – Уитни (U-критерий). Расчет рангового коэффициента корреляции Спирмена (r) позволял определить интенсивность корреляционной связи. Сравнение качественных показателей в группах производилось при помощи расчета хи-квадрата (χ2) Пирсона.
Результаты и их обсуждение
Для достижения поставленной цели все пациенты в зависимости от степени стеноза коронарных артерий были разделены на две группы: 24 пациента (1 группа) с умеренным атеросклеротическим поражением коронарных артерий (стеноз 21–70 %) и 39 пациентов (2 группа) с выраженным поражением коронарных артерий (стеноз ≥71 %). В таблице 1 представлена краткая сравнительная клиническая характеристика групп пациентов. Приведенные в таблице 1 данные демонстрируют отсутствие статистически значимых различий по сравниваемым показателям.
Таблица 1
Table 1
Клиническая характеристика пациентов исследуемых групп
Clinical characteristics of patients in the study groups
Показатель | 1 группа | 2 группа |
Возраст, годы | 56,4 [48; 63] | 57,8 [48; 64] |
Длительность анамнеза ИБС, годы | 3,5 [2; 5] | 3,8 [2; 6] |
ФК стенокардии | ||
2, n (%) | 21 (87,5 %) | 27 (69 %) |
Показатель | 1 группа | 2 группа |
3, n (%) | 3 (12,5 %) | 12 (31 %) |
Стадия ХСН | ||
I–II A, n (%)* | 20 (95 %) | 36 (92 %) |
II Б–III, n (%) | 1 (5 %) | 3 (8 %) |
ФК ХСН (NYHA) | ||
II, n (%) | 19 (90 %) | 32 (82 %) |
III, n (%) | 2 (10 %) | 6 (18 %) |
Примечание: р1 – уровень статистической значимости различий с 1 группой.
Представленные в таблице 2 данные демонстрируют статистически значимую разницу по показателю ОФИК в сравниваемых группах. В группе пациентов с выраженным поражением коронарных артерий показатель ОФИК был статистически значимо выше, чем в группе пациентов с умеренным атеросклеротическим поражением коронарных артерий (р = 0,019). При этом в обеих группах он превышал референсные значения (2–6 %), что свидетельствует об активации процессов фиброзообразования во внеклеточном матриксе миокарда у пациентов с ишемической болезнью сердца: стабильной стенокардией напряжения и сохраненной систолической функцией левого желудочка. Этот процесс на микроуровне представляется следующим образом. Чем больше степень стеноза коронарных артерий, тем больше гипоксические изменения и окисидативный стресс. Накопление продуктов окисления в миокарде, снижение адаптационных механизмов приводит к активации иммунной системы с развитием провоспалительного и профибротического состояний, которые вызывают структурные, а затем и функциональные изменения миокарда. В этих изменениях ключевую роль играет семейство факторов роста фибробластов, способствуя гипертрофии и фиброзу миокарда через стимуляцию митогенактивируемых протеинкиназ и регуляцию активности α-Klotho (независимого от α-Klotho кальцинурин-/ядерного фактора активированных Т-клеток), который ингибирует фиброзирование внеклеточного матрикса миокарда, индуцированный ангиотензином II, трансформирующим фактором роста-β1 и гиперфосфатемией [Мясоедова, 2017; Калинкина и др., 2021; Frangogiannis, 2021]. Полученные нами результаты говорят о том, что чем больше стеноз коронарных артерий, тем активнее протекает процесс фиброзирования внеклеточного матрикса миокарда.
Таблица 2
Table 2
Показатели объёмной фракции интерстициального коллагена миокарда в сравниваемых группах
Indicators of the volume fraction of interstitial myocardial collagen in the compared groups
Показатель/ | 1 группа | 2 группа |
ОФИК, % | 7,9 [6,8; 10,1] | 9,8 [7,4; 11,6] |
Примечание: р1 – уровень статистической значимости различий с 1 группой.
Важным аспектом изучения фиброзирования миокарда является не только оценка его наличия и степени выраженности, но и рассмотрение взаимосвязи со структурно-функциональными показателями сердца. Известно, что нарушение баланса обмена коллагена во внеклеточном матриксе миокарда вызывает нарушение электрофизиологических механизмов в кардиомиоцитах, приводит к развитию диастолической дисфункции левого желудочка, а при прогрессировании процесса – и к систолической дисфункции [Шевченко, Ульбашев, 2022; Zhu et al., 2022]. Согласно клиническим рекомендациям по лечению и диагностике пациентов с ХСН, помимо изучения по данным ЭХОКГ диастолической функции и систолической функции ЛЖ путем расчёта ФВ ЛЖ, предлагается производить с использованием спекл-трекинг технологии оценку глобальной продольной систолической деформации ЛЖ, так как этот показатель на ранних стадиях позволяет оценить формирующееся контрактильные и гемодинамические изменения миокарда. Это обусловлено тем, что наиболее чувствительны к ишемии субэндокардиальные продольно расположенные мышечные волокна ЛЖ, следовательно, с них и начинается продольное деформационное ремоделирование ЛЖ [Гриценко и др., 2021; Базилевич и др., 2022].
Оценка показателя GLS в сравниваемых группах показала, что во 2 группе пациентов изучаемый показатель статистически значимо отличался от группы пациентов с умеренным атеросклеротическим поражением коронарных артерий (р = 0,016) (табл. 3). При этом в 1 группе пациентов Ме показателя GLS находилась в пределах референсных значений [Фозилов и др., 2021; Пономаренко и др., 2023].
Таблица 3
Table 3
Показатель GLS в сравниваемых группах
The GLS indicator in the compared groups
Показатель/ | 1 группа | 2 группа |
GLS, % | –19,2 [–16,1; –23,6] | –15,3 [–11,3; –17,7] |
Примечание: р1 – уровень статистической значимости различий с 1 группой.
Показатель ОФИК и показатель GLS в обеих группах пациентов имели прямые статистически значимые связи, при этом в группе пациентов с выраженным поражением коронарных артерий она была сильнее (r=0,63, р=0,031), чем в группе пациентов с умеренным атеросклеротическим поражением коронарных артерий (r=0,56, р=0,039). То есть, чем больше показатель ОФИК, а, следовательно, и интерстициальный фиброз миокарда левого желудочка, тем более значимо нарушается глобальная продольная систолическая деформация ЛЖ.
Заключение
У пациентов с ишемической болезнью сердца: стабильной стенокардией напряжения и сохраненной систолической функцией ЛЖ показатель степень интерстициального фиброзирования миокарда ЛЖ, оцененная по показателю ОФИК, зависит от степени стеноза коронарных артерий. При прогрессировании атеросклеротического процесса в коронарных артериях степень фиброзирования миокарда ЛЖ увеличивается, что ассоциируется с усилением нарушения глобальной продольной систолической деформации ЛЖ.


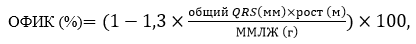



Reference lists
Abdrakhmanova A.I., Amirov N.B., Tsibul'kin N.A., Kashapov L.R., Oslopova Yu.V., Khabibullin I.M., Gornaeva L.I., Galimzyanova L.A. 2020. Vozmozhnosti koronaroangiografii v diagnostike porazheniya koronarnykh arteriy u patsientov s bezbolevoy ishemiey miokarda [Possibilities of Coronary Angiography in the Diagnosis of Coronary Artery Disease in Patients with Painless Myocardial Ischemia]. Sovremennye problemy nauki i obrazovaniya. 4. URL: https://science-education.ru/ru/article/view?id=30058 (data obrashcheniya: 21.08.2023).
Bazilevich A.V., Nelasov N.Ju., Sidorov R.V., Doltmurzieva N.S., Borshhev G.G., Pospelov D.Ju., Ovrulova M.M. 2022. Sovremennye vozmozhnosti jehokardiografii pri hirurgicheskom lechenii bol'nyh IBS [Modern Possibilities of Echocardiography in Surgical Treatment of Patients with Coronary Heart Disease]. Vestnik Nacional'nogo mediko-hirurgicheskogo Centra im. N.I. Pirogova. 17: 78–81. doi: 10.25881/20728255-2022-17-2-78
Bojcov S.A. 2022. Hronicheskaja serdechnaja nedostatochnost': jevoljucija jetiologii, rasprostranennosti i smertnosti za poslednie 20 let [Chronic Heart Failure: Evolution of Etiology, Prevalence and Mortality over the Past 20 Years]. Terapevticheskij arhiv. 94(1): 5–8. doi: 10.26442/00403660.2022.01.201317
Gordeeva M.S., Parmon E.V., Karlina V.A., Ryzhkova D.V. 2022. Fragmentacija QRS-kompleksa kak marker fibroza miokarda u pacientov s ishemicheskoj bolezn'ju serdca [Fragmentation of the QRS Complex as a Marker of Myocardial Fibrosis in Patients with Ischemic Heart Disease. Science and Innovation in Medicine]. Nauka i innovacii v medicine. 2: 95–102. doi: 10.35693/2500-1388-2022-7-2-95-102
Gritsenko O.V., Chumakova G.A., Trubina E.V. 2021. Vozmozhnosti speckle-tracking ekhokardiografii dlya diagnostiki disfunktsii miokarda [Possibilities of Speckle-Tracking Echocardiography for Diagnosing Myocardial Dysfunction]. CardioSomatika. 12(1): 5–10. doi: 10.26442/22217185.2021.1.200756
Kalinkina T.V., Lareva N.V., Chistjakova M.V., Sten'kina V.K., Puncokdashina T.B. 2021. Opyt primenenija rascheta ob'emnoj frakcii intersticial'nogo kollagena u bol'nyh arterial'noj gipertoniej [Experience of Using the Calculation of the Volume Fraction of Interstitial Collagen in Patients with Arterial Hypertension]. Sibirskoe medicinskoe obozrenie. 1: 90–95. doi: 10.20333/2500136-2021-1-90-95
Mironova O.Ju., Isaev G.O., Berdysheva M.V., Shahnovich R.M., Fomin V.V. 2023. Sovremennye metodiki ocenki fiziologicheskoj znachimosti stenozirujushhih porazhenij koronarnyh arterij [Modern Methods for Assessing the Physiological Significance of Stenotic Lesions of the Coronary Arteries]. Terapevticheskij arhiv. 95(4): 341–346. doi: 10.26442/00403660.2023.04.202169
Muhametgareeva A.V., Kashtalap V.V., Molchanov A.N., Vorob'ev A.S., Urvanceva I.A., Romashkin V.V., Kovalenko L.V. 2020. Vozmozhnosti ispol'zovanija ul'trazvukovoj ocenki deformacii miokarda levogo zheludochka v kardiologii [Possibilities of Using Ultrasound Assessment of Left Ventricular Myocardial Deformation in Cardiology]. Ul'janovskij mediko-biologicheskij zhurnal. 3: 28–43. doi: 10.34014/2227-1848-2020-3-28-43
Myasoedova E.I. 2017. Fraktsiya fibroza miokarda i strukturnoe remodelirovanie levykh otdelov serdtsa u patsientov s ishemicheskoy kardiomiopatiey [Myocardial Fibrosis Fraction and Structural Remodeling of the Left Heart in Patients with Ischemic Cardiomyopathy]. Astrakhanskiy meditsinskiy zhurnal. 2017. 12(2): 98–103.
Ponomareva O.V., Smirnova E.A. 2024. Sovremennyy vzglyad na rol' fibroza miokarda i ego biokhimicheskikh markerov v diagnostike khronicheskoy serdechnoy nedostatochnosti [A Modern View on the Role of Myocardial Fibrosis and its Biochemical Markers in the Diagnosis of Chronic Heart Failure]. Nauka molodykh (Eruditio Juvenium). 12(2): 303–316. doi: 10.23888/HMJ2024122303-316
Ponomarenko I.V., Sukmanova I.A., Sanaeva A.K., Trubina E.V., Narenkova S.O. 2023. Vozmozhnosti speckle-tracking-jehokardiografii v diagnostike subklinicheskoj disfunkcii levogo zheludochka [The Potential of Speckle-Tracking Echocardiography in the Diagnosis of Subclinical Left Ventricular Dysfunction]. Kardiologija: novosti, mnenija, obuchenie. 11(2): 22–29. doi:10.33029/2309-1908-2023-11-2-22-29
Tarasova I.V., Vertkin A.L., Kozhushkov V.A., Kozhushkov I.A., Chebotar' N.E., Geydarova E.M. 2023. Obzor vizualiziruyushchikh metodov issledovaniya, primenyaemykh v diagnostike stabil'noy ishemicheskoy bolezni serdtsa [A Review of Imaging Research Methods Used in the Diagnosis of Stable Coronary Heart Disease]. Lechashchiy Vrach. 4(26): 48–55. doi: 10.51793/OS.2023.26.4.007
Usacheva E.V., Nelidova A.V., Kulikova O.M., Fljanku I.P. 2021. Smertnost' trudosposobnogo naselenija Rossii ot serdechno-sosudistyh zabolevanij [Mortality of the Working-Age Population of Russia from Cardiovascular Diseases]. Gigiena i sanitarija. 100(2): 159–165. doi: 10.47470/0016-9900-2021-100-2-159-165
Fozilov Kh.G., Shek A.B., Bekmetova F.M., Alieva R.B., Mukhamedova M.G., Mullabaeva G.U., Donierov Sh.N., Ilkhomova L.T., Bekmetova S.I., Khotamova M.N. 2021. Osobennosti deformatsionnykh svoystv levogo zheludochka u bol'nykh c porazheniem koronarnykh arteriy [Features of the Deformation Properties of the Left Ventricle in Patients with Lesions of the Coronary Arteries]. Klinicheskaya i eksperimental'naya khirurgiya. Zhurnal imeni akademika B.V. Petrovskogo. 9(3): S. 118–124. doi: 10.33029/2308-1198-2021-9-3-118-124
Shevchenko Ju.L., Ul'bashev D.S. 2022. Immobilizirujushhij intersticial'nyj fibroz serdca. Chast' 1 [Immobilizing Interstitial Fibrosis of the Heart. Part 1]. Vestnik Nacional'nogo mediko-hirurgicheskogo Centra im. N.I. Pirogova. 2: 4–10. doi: 10.25881/20728255-2022-17-2-4
Fan J.L., Su B., Zhao X., Zhou B.Y., Ma C.S., Wang H.P., Hu, S.D., Zhou Y.F., Ju, Y.J., Wang M.H. 2020. Correlation of Left Atrial Strain with Left Ventricular End-Diastolic Pressure in Patients with Normal Left Ventricular Ejection Fraction. Int. J. Cardiovasc. Imaging. 36: 1659–1666. doi: 10.1007/s10554-020-01869-7
Frangogiannis N.G. 2021. Cardiac Fibrosis. Cardiovasc. Res. 117(6): 1450–1488. doi: 10.1093/cvr/cvaa324
Schimmel K., Ichimura K., Reddy S., Haddad F., Spiekerkoetter E. 2022. Cardiac Fibrosis in the Pressure Overloaded Left and Right Ventricle as a Therapeutic Target. Front. Cardiovasc. Med. 9: 886553. doi: 10.3389/fcvm.2022.886553
Shirani J., Pick R., Quo Y. 1992. Usefulness of the Electrocardiogram and Echocardiogram in Predicting the Amount of Patients with Chronic Heart Failure. Am. J. Cardiol. 69: 1502.
Zhu L., Wang Y., Zhao S., Lu M. 2022. Detection of Myocardial Fibrosis: Where We Stand. Front. Cardiovasc. Med. 9: 926378. doi: 10.3389/fcvm.2022.926378