Современный малоинвазивный способ лечения редкого осложнения после лапароскопической рефундопликации с аллопластикой
Aннотация
Хирургическое лечение пациентов с грыжами пищеводного отверстия диафрагмы наиболее часто представляет из себя лапароскопическую фундопликацию Лапароскопическая фундопликация, по данным различных литературных источников, имеет от 10 % до 50 % рецидива заболевания. Осложнения, характерные для антирефлюксной хирургии, включают пневмоторакс, гастроэзофагеальные или гепатолиенальные травмы и дисфагию. Использование различных сетчатых имплантатов при выполнении рефундопликации является дискутабельным вопросом, а случаев лечения осложнений в результате использования различных сетчатых имплантатов в рецидивной антирефлюксной хирургии описано крайне мало. Комбинированный и мультидисциплинарный подход позволяет купировать различные осложнения, зачастую малоинвазивным способом.
Ключевые слова: грыжа пищеводного отверстия диафрагмы, сетчатый имплант, биологический имплант, абсцесс, рецидивная грыжа, лапароскопическая фундопликация, антирефлюксная хирургия
Введение
Грыжа пищеводного отверстия диафрагмы является распространенным структурным дефектом пищеводного отверстия с различными симптомами, начиная от изжоги и заканчивая дисфагией. Большинство из этих грыж небольшие, они часто бессимптомны, примерно 95 % составляет грыжа 1 типа. Лечение консервативное плюс изменение образа жизни, при этом хирургическое вмешательство используется в случаях, когда вышеупомянутое оказывается неэффективным. Хотя лапароскопическая операция на грыже с помощью крурорафии и фундопликации стала стандартной практикой, рецидивы грыж пищеводного отверстия диафрагмы после хирургического вмешательства являются обычным явлением с зарегистрированным уровнем в диапазоне от 10 до 50 % [Geerts, 2024].
За последнее десятилетие используются несколько способов лечения грыжи пищеводного отверстия диафрагмы, включая открытую хирургию, лапароскопию (Nissen, Toupet, Dor fundoplication), трансоральную фундопликацию без разреза (TIF), другие медицинские подходы, такие как изменение образа жизни, лекарственная терапия [Singhal et al., 2024].
Среди этих методов два технических аспекта, которые могут повлиять на результат, все еще обсуждаются: круропластика с сеткой и выбор между
360-градусной фундопликацией Nissen и 270-градусной фундопликацией Toupet [Köckerling et al., 2020].
Фундопликация по Toupet с пластикой сеткой и без нее была операцией выбора при рецидивных грыжах пищеводного отверстия диафрагмы для минимизации риска послеоперационной дисфагии и синдрома газового вздутия [Panici et al., 2024].
Несмотря на развитие современных хирургических технологий, количество и высокая вариабельность осложнений лапароскопического лечения пациентов с грыжей̆ пищеводного отверстия сохраняется [Бородкин и др., 2022].
Хирургические осложнения, как правило, незначительны и не связаны непосредственно с самой операцией. Общий 30-дневный уровень смертности, связанный с антирефлюксной операцией, составляет примерно 0,19 %. Осложнения, характерные для антирефлюксной хирургии, включают пневмоторакс, гастроэзофагеальные или гепатолиенальные травмы и дисфагию. Пневмоторакс является наиболее распространенным интраоперационным осложнением, но сообщается, что он встречается менее чем у 2 % пациентов. Травмы желудка или пищевода возникают примерно у 1 % пациентов, подвергающихся фундопликации Nissen. Травмы селезенки и печени могут привести к кровотечению и возникнуть примерно у 2,3 % пациентов. Серьезная гепатолиенальная травма встречается редко. Дисфагия обычно проходит без дальнейшего вмешательства и чаще всего вызывается послеоперационным отеком [Smith et al., 2025].
Описание клинического случая
Больной К., 54 года, поступил в экстренном порядке в отделение неотложной хирургической помощи ММНКЦ им С.П. Боткина с интоксикационным синдромом, жалобами на затруднение прохождения твердой пищи. Из анамнеза стало известно, что два месяца назад был повторно оперирован в Германии по поводу рецидивной грыжи пищеводного отверстия диафрагмы. Установлен саморассасывающийся сетчатый имплант. Жалобы возникли через месяц после вмешательства.
По результатам лабораторных показателей отмечен лейкоцитоз со сдвигом лейкоцитарной формулы влево. Повышение СРБ до 156 мг/л. Других отклонений по лабораторным показателям не выявлено.
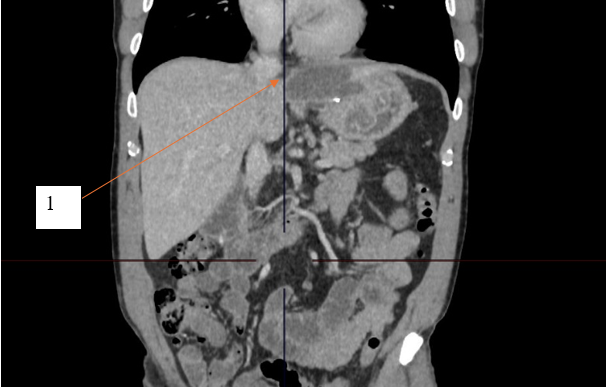
По данным компьютерной томографии органов брюшной полости с внутривенным контрастированием выявлена структура жидкостной плотности в области кардиального отдела желудка без убедительной связи с просветом желудка. Единичные увеличенные параэзофагельные, паракавальные, парааортальные лимфоузлы. Другой патологии не выявлено. Результаты компьютерной томографии с внутривенным контрастированием представлены на рисунках 1 и 2.
Рис. 1. Компьютерная томограмма с внутривенным контрастным усилением, пациент К., 54 года, фронтальный срез, отсроченная фаза. 1 – структура жидкостной плотности в области кардиального отдела желудка
Fig. 1. Computed tomogram with intravenous contrast enhancement, patient K., 54 years old, frontal section, delayed phase. 1 – liquid density structure in the cardiac region of the stomach
После обсуждения пациента на междисциплинарном консилиуме принято решение о выполнении эндосонографии желудка, с интраоперационным решением вопроса об объёме вмешательства. 11.04.2025 эхоэндоскоп свободно проведен в желудок, при обзорном сканировании из просвета в верхней трети желудка парагастрально визуализировано жидкостное скопление овоидной формы размерами 32 мм на 24 мм. С гиперэхогенной капсулой, с гетерогенным содержимым внутри. Принято решение о формировании цисто-гастроанастомоза. Под ЭУС-контролем выполнена пункция кистозного образования. Получен пунктат гнойного характера. Отправлен для посева на флору и чувствительность к антибиотикам. В просвет кисты введен контраст. По струне-проводнику пункционный канал расширен с помощью цистотома 8Fr. По проводнику под рентгеноскопическим, эндоскопическим и ЭУС-контролем установлен нитиноловый покрытый эндопротез MI Tech 120 мм. на 30 мм. После раскрытия стента в просвет желудка одномоментно было эвакуировано до 100,0 мл мутного гнойного содержимого.
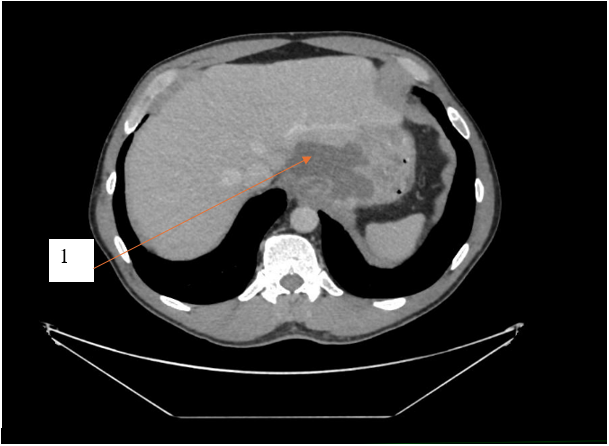
Рис. 2. Компьютерная томограмма с внутривенным контрастным усилением, пациент К., 54 года, аксиальный срез, отсроченная фаза. 1 – структура жидкостной плотности в области кардиального отдела желудка
Fig. 2. Computed tomogram with intravenous contrast enhancement, patient K., 54 years old, axial section, delayed phase. 1 – liquid density structure in the cardiac region of the stomach
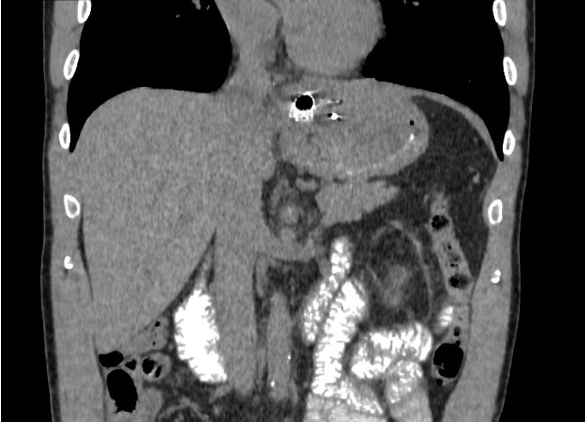
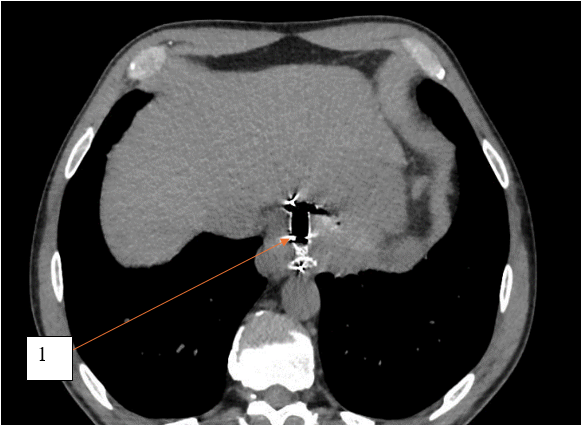
При контрольной рентгеноскопии на вторые сутки наблюдения отмечено уменьшение полости кисты, без затеков контрастного вещества, раскрытие стента удовлетворительное, до 50 % на уровне талии. Талия по центру. Течение послеоперационного периода гладкое, однако отмечалось наличие синхронного трепетания диафрагмы (singultus) вследствие раздражения нитиноловым стентом. По результатам контрольной компьютерной томографии органов брюшной полости с контрастированием, выполненной на третьи сутки после операции, стент определялся на уровне кардиального отдела желудка. Ранее выявленный жидкостной коллектор достоверно не визуализировался. Затеков ранее принятого контрастного йодсодержащего препарата за пределы стента не отмечено. Результаты контрольной компьютерной томографии представлены на рисунках 3 и 4.
По результатам контрольных лабораторных показателей отмечена нормализация показателей маркеров воспаления и белков острой фазы.
Учитывая отсутствие жидкостного скопления, а также наличие не купируемой икоты, принято решение об удалении стента. 15.04.2025 г. выполнено эндоскопическое вмешательство, при котором эндоскоп был свободно проведен по пищеводу в желудок. В проекции кардиального отдела желудка определялся дистальный край ранее установленного саморасширяющегося стента. На момент осмотра поступления гноя отмечено не было. Ранее фиксированная металлическая конструкция инструментально извлечена. При контрольном осмотре выявлена небольшая очищенная полость. Края последней максимально сведены с помощью шести эндоскопических клипс. С целью контроля после операции эндоскопического удаления нитинолового стента с эндоскопическим сведением краев полости металлическими клипсами выполнена контрольная рентгеноскопия желудка с глотком йодсодержащего контрастного вещества.
Рис. 3. Компьютерная томограмма с пероральным и внутривенным контрастным усилением, пациент К., 54 года, фронтальный срез. 1 – стент на уровне кардиального отдела желудка
Fig. 3. Computed tomography with oral and intravenous contrast enhancement, patient K., 54 years old, frontal section. 1 – stent at the level of the cardiac part of the stomach
Рис. 4. Компьютерная томограмма с пероральным и внутривенным контрастным усилением, пациент К., 54 года, аксиальный срез. 1 – стент на уровне кардиального отдела желудка
Fig. 4. Computed tomogram with oral and intravenous contrast enhancement, patient K., 54 years old, axial section. 1 – stent at the level of the cardiac part of the stomach
Затека контрастного вещества не получено. Результаты контрольной рентгеноскопии представлены на рисунке 5.
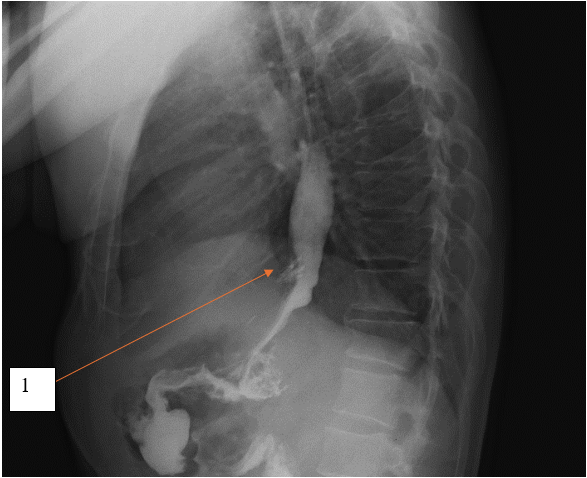
Рис. 5. Рентгеноскопия с водорастворимым контрастным усилением, пациент К., 54 года, боковая проекция. 1 – признаков экстравазации нет, эндоскопические клипсы состоятельны
Fig. 5. X-ray examination with water-soluble contrast enhancement, patient K., 54 years old, lateral projection. 1 – no signs of extravasation, endoscopic clips are sound
После контрольной рентгеноскопии пациент выписан из стационара на амбулаторный этап лечения и наблюдения.
Обсуждение
Рецидив грыжи пищеводного отверстия диафрагмы – довольно частая проблема после ранее выполненных антирефлюксных вмешательств [Panici et al., 2024]. Далеко не всегда стоит прибегать к повторным хирургическим операциям. Показания к повторной операции в данном случае должны сочетаться с рецидивом гастроэзофагеального рефлюкса, подтвержденным данными pH метрии, наличии параэзофагеального компонента либо миграции других органов через пищеводное отверстие диафрагмы в заднее средостение. Само по себе наличие антирефлюксной манжеты в заднем средостении не является показанием к повторному хирургическому вмешательству, а может быть расценено как вариант нормального течения послеоперационного периода, особенно при вторично укороченном пищеводе. Вариант использования имплантов (сетчатых или биологических) с целью ликвидации больших дефектов пищеводного отверстия диафрагмы – вопрос дискутабельный. Имеет как своих сторонников, так и противников [Singhal et al., 2024]. Немаловажным аспектом являются осложнения, связанные с имплантами, в зоне пищеводного отверстия диафрагмы в виде нагноения или миграции инородных тел в просвет желудочно-кишечного тракта [Panici et al., 2024]. Учитывая трудную доступность зоны пищеводного отверстия диафрагмы для ревизии и дренирования, всегда возникают большие сложности в разрешении данных осложнений, как правило, требующих мультидисциплинарного подхода.
В данном клиническом случае представлен малоинвазивный способ лечения редкого послеоперационного осложнения у больного, перенесшего рефундопликацию с аллопластикой.
Частичная фундопликация предпочтительнее у пациентов с известной гипомоторностью пищевода или нарушенным перистальтическим резервом при возникновении послеоперационной дисфагии [Yadlapati et al., 2022].
В случае, когда большой размер грыжевого дефекта препятствует первичному сшиванию без натяжения, использование композитной сетки может обеспечить эффективное одновременное восстановление. Тем не менее при размещении сетки необходимо соблюдать осторожность, чтобы избежать повреждения аорты и перфораций пищевода, вызванных эрозией сетки [Muramatsu et al., 2022].
Применение сетки снижает риск рецидива и связанной с ним необходимости повторной операции после ушивания дефекта пищеводного отверстия диафрагмы больших размеров (> 5 см), в то время как общий уровень осложнений не меняется. Таким образом, преимущества перевешивают риск осложнений, связанных с сеткой, особенно учитывая сложность повторных операций при рецидивных грыжах пищеводного отверстия диафрагмы. При использовании синтетической сетки следует использовать быстро интегрирующийся материал, такой как полипропилен. Фиксация сетки с помощью фибринового клея может быть предпочтительнее других форм фиксации сетки [Nickel et al., 2023].
Заключение
Несмотря на различные мнения экспертов касательно использования сетчатых имплантов в первичной и повторной антирефлюксной хирургии, строгих критериев к применению сетчатых имплантатов антирефлюксной хирургии нет. Таким образом, в случае наличия у больного большого дефекта в области пищеводного отверстия диафрагмы для более надежной реконструкции, а также в случае рецидивной антирефлюксной хирургии могут быть использованы как композитные, так и биоразлагаемые сетчатые протезы.
В случае использования сетки требуется особое внимание уделить критериям выбора материала сетчатого имплантата и способу ее фиксации для предупреждения послеоперационных осложнений, связанных с перфорацией пищевода или желудка. В случае же лечения осложнений в позднем послеоперационном периоде применение малоинвазивных способов предпочтительнее с учетом отсутствия рецидива грыжи. В данном клиническом случае формирование и последующее эндоскопическое закрытие цисто-гастроанастомоза позволило решить проблему интоксикационного синдрома и дисфгагии у пациента, а малоинвазивные методики лечения позволили сократить сроки пребывания больного в стационаре.





Список литературы
Бородкин И.Н., Демин Д.Б., Лященко С.Н., Файзулина Р.Р., Савин Д.В. 2022. Осложнения лапароскопических вмешательств при грыжах пищеводного отверстия диафрагмы. Эндоскопическая хирургия. 28(1): 57–64. doi: 10.17116/endoskop20222801157
Geerts J.H., de Haas JWA., Nieuwenhuijs V.B. 2024 Lessons Learned from Revision Procedures: A Case Series Pleading for Reinforcement of the Anterior Hiatus in Recurrent Hiatal Hernia. Surg Endosc. May; 38(5): 2398–2404. doi: 10.1007/s00464-024-10703-3. Epub 2024 Apr 2. PMID: 38565689; PMCID: PMC11078792.
Köckerling F., Zarras K., Adolf D., Kraft B., Jacob D., Weyhe D., Schug-Pass C. 2020. What Is the Reality of Hiatal Hernia Management? -A Registry Analysis. Front Surg. Oct 22; 7: 584196. doi: 10.3389/fsurg.2020.584196. PMID: 33195390; PMCID: PMC7642514.
Muramatsu R., Nobuoka T., Ito T., Ogawa T., Korai T., Takemasa I. 2022 Laparoscopic Mesh Repair and Toupet Fundoplication for Parahiatal Hernia Complicated by Sliding Hiatal Hernia: A Case Report. Int J Surg Case Rep. Nov; 100: 107664. doi: 10.1016/j.ijscr.2022.107664. Epub 2022 Sep 14. PMID: 36270209
Nickel F., Müller P.C., Cizmic A., Häberle F., Muller M.K., Billeter A.T., Linke G.R., Mann O., Hackert T., Gutschow C.A., Müller-Stich B.P. 2023. Evidence Mapping on How to Perform an Optimal Surgical Repair of Large Hiatal Hernias. Langenbecks Arch Surg. Dec 21; 409(1): 15. doi: 10.1007/s00423-023-03190-y. PMID: 38123861; PMCID: PMC10733223.
Panici Tonucci T., Aiolfi A., Bona D., Bonavina L. 2024. Does Crural Repair with Biosynthetic Mesh Improve Outcomes of Revisional Surgery for Recurrent Hiatal Hernia? Hernia. Oct; 28(5): 1687–1695. doi: 10.1007/s10029-024-03023-x. Epub 2024 Mar 29. PMID: 38551795; PMCID: PMC11450103.
Singhal V.K., Md Suleman A., Senofer N., Singhal V.V. 2024. Current Trends in the Management of Hiatal Hernia: A Literature Review of 10 Years of Data. Cureus. Oct 20; 16(10): e71921. doi: 10.7759/cureus.71921. PMID: 39564064; PMCID: PMC11575107.
Smith R.E., Sharma S., Shahjehan R.D. 2024. Hiatal Hernia. Jul 17. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan–. PMID: 32965871.
Yadlapati R., Gyawali C.P., Pandolfino J.E. 2022. CGIT GERD Consensus Conference Participants. AGA Clinical Practice Update on the Personalized Approach to the Evaluation and Management of GERD: Expert Review. Clin Gastroenterol Hepatol. May; 20(5): 984–994.e1. doi: 10.1016/j.cgh.2022.01.025. Epub 2022 Feb 2. Erratum in: Clin