Рентгенохирургическая коррекция стриктур билиодигестивных анастомозов, осложненных холелитиазом
Aннотация
Цель исследования – оценка безопасности, эффективности и риска развития рецидива стриктуры билиодигестивного анастомоза при его антеградной рентгенохирургической коррекции. Группу исследования составили 16 пациентов со стриктурами билиодигестивного анастомоза, осложненными холелитиазом, контрольную – 42 пациента со стриктурами анастомоза без сопутствующего холелитиаза. Больным была проведена антеградная баллонная реконструкция стриктуры с низведением дренажа за зону анастомоза и сохранением его в качестве стента на срок не менее 9 месяцев. В течение 5 лет наблюдения рецидив стриктуры, потребовавший повторного рентгенохирургического вмешательства у больных контрольной группы, возник в 5 случаях (11,9 %), в группе исследования – в 9 случаях (56,3 %). Достоверность результатов лечения оценивалась методиками непараметрической статистики. Риск рецидива стриктуры у пациентов с сопутствующим холелитиазом оказался достоверно выше. Чрескожное чреспеченочное разрешение холелитиаза, сопутствующего рубцовой стриктуре билиодигестивного анастомоза, с использованием методики антеградной контактной литотрипсии и литоэкстракции оправдано прежде всего у больных с высоким операционным риском.
Ключевые слова: билиодигестивный анастомоз, рубцовая стриктура анастомоза, баллонная дилатация стриктуры, холелитиаз, антеградное наружно-внутреннее дренирование желчного дерева, антеградная литотрипсия
Введение
Вероятность возникновения стриктуры сформированного билиодигестивного анастомоза (БДА) колеблется в широком диапазоне – от 4,1 % до 69 %. Чаще всего риск развития стриктуры оценивают в 10–20 % в течение 11–30 месяцев после операции [Schreuder et al., 2020; Giuliant et al., 2023; Nagai et al., 2024; Yung et al., 2024]. Эндоскопические методики (рассечение, баллонная дилатация, стентирование) формируют основу современного подхода к лечению доброкачественных стриктур БДА. При безуспешности или невозможности эндоскопического пособия используются чрескожные рентгенохирургические методики внутреннего или наружного билиарного дренирования, баллонной дилатации и стентирования [Fang et al., 2021; Ye et al., 2021; Fan et al., 2022; Sato et al., 2022; Colombo et al., 2023; Ashat et al., 2024].
Ретроградный доступ к зоне анастомоза может быть реализован и эндоскопически с использованием двухбаллонной методики энтероскопии [Sato et al., 2020; Nagakawa et al., 2021; Choi et al., 2023]. Кроме того, классической является методика создания gastric access loop во время первичного формирования билиодигестивного анастомоза для эндоскопического доступа к нему в случае развития стриктуры [Raafat et al., 2023]. Антеградный чрескожный чреспеченочный рентгенохирургический доступ с баллонным восстановлением проходимости анастомоза и последующим продолженным каркасным дренированием зоны стриктуры БДА является признанным миниинвазивным способом лечения данной патологии [Кулезнева и др., 2021; Li et al., 2020; Nunes et al., 2022; Mie et al., 2024].
Ограничением к использованию рентгенохирургических методик в лечении стриктур БДА является невозможность антеградной реканализации стриктуры (до 25 % случаев), недостаточная дилатация желчного дерева, а также крупные конкременты, располагающиеся проксимальнее анастомоза [Chikamori et al., 2022; Suzuki et al., 2024]. Более того, холелитиаз, сопутствующий стриктуре БДА, традиционно является одной из основных причин отказа от миниинвазивного ретроградного или антеградного способа коррекции патологии в пользу повторного реконструктивного вмешательства.
Цель исследования: оценка безопасности, непосредственной эффективности и риска развития рецидива стриктуры БДА при его антеградной рентгенохирургической коррекции с разрешением сопутствующего холелитиаза.
Объект и методы исследования
Группу исследования составили 16 пациентов со стриктурами БДА, осложненными холелитиазом. В трех случаях удалось низвести конкременты общего печеночного протока в отводящую кишку после баллонной дилятации стриктуры БДА. В 13 наблюдениях при мегахолелитиазе потребовалась этапная модификация пункционного холангиостомического доступа в чрескожный рентгенохирургический доступ диаметром 9 мм для последующей контактной механической и пневматической литотрипсии и литоэкстракции (рис. 1–5).
Контрольную группу составили 42 пациента со стриктурами БДА без сопутствующего холелитиаза. Больным была проведена антеградная рентгенохирургическая коррекция зоны стриктуры по классической методике. Последняя предполагала последовательный чрескожный чреспеченочный доступ в желчное дерево под ультразвуковым и рентгеновским контролем с последующей этапной баллонной реконструкцией стриктуры БДА, низведением дренажа за зону анастомоза и сохранением его в качестве стента. Наружно-внутреннее дренирование желчного дерева пролонгировалось на срок не менее 9 месяцев с контрольными баллонными ревизиями зоны БДА.
Для оценки достоверности различий результатов лечения пациентов в обеих группах использовались методики непараметрической статистики. Была сформулирована «нулевая гипотеза» – частота пятилетних рецидивов стриктуры БДА после ее рентгенохирургической коррекции не зависит от наличия сопутствующего холелитиаза. Для определения характера статистической связи и ее силы между анализируемыми качественными параметрами, а также проверки достоверности этой связи при p ≤ 0,05 вычисляли коэффициенты ассоциации Юла и контингенции Пирсона с оценкой результата по шкале Чеддока. При этом сравнивали 2 выборки: первая включала в себя наблюдения рентгенохирургической коррекции стриктуры БДА без сопутствующего холелитиаза (n – 42, 5-летних рецидивов – 5), вторая – пациентов с холелитиазом на фоне стриктуры БДА (n – 16, 5-летних рецидивов – 7). Оценка кумулятивных показателей частоты рецидива стриктуры БДА с учетом наличия и отсутствия сопутствующего холелитиаза проводилась по методике Каплана – Мейера.
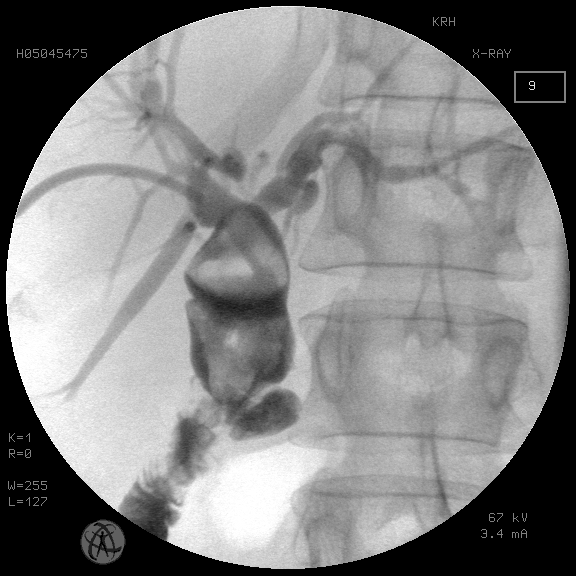
Рис. 1. Множественный мегахолангиолитиаз проксимальнее стриктуры БДА. Состояние после чрескожной чреспеченочной холангиостомии
Fig. 1. Multiple megacholangiolithiasis proximal to the stricture of the BDA. Condition after percutaneous transhepatic cholangiostomy
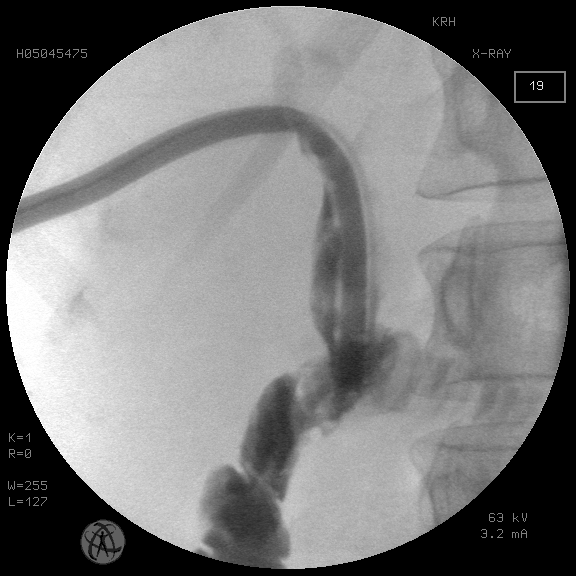
Рис. 2. То же наблюдение, состояние после чреспеченочной холангиостомии большого диаметра и частичной литотрипсии
Fig. 2. The same observation. Сondition after large-diameter transhepatic cholangiostomy and partial lithotripsy
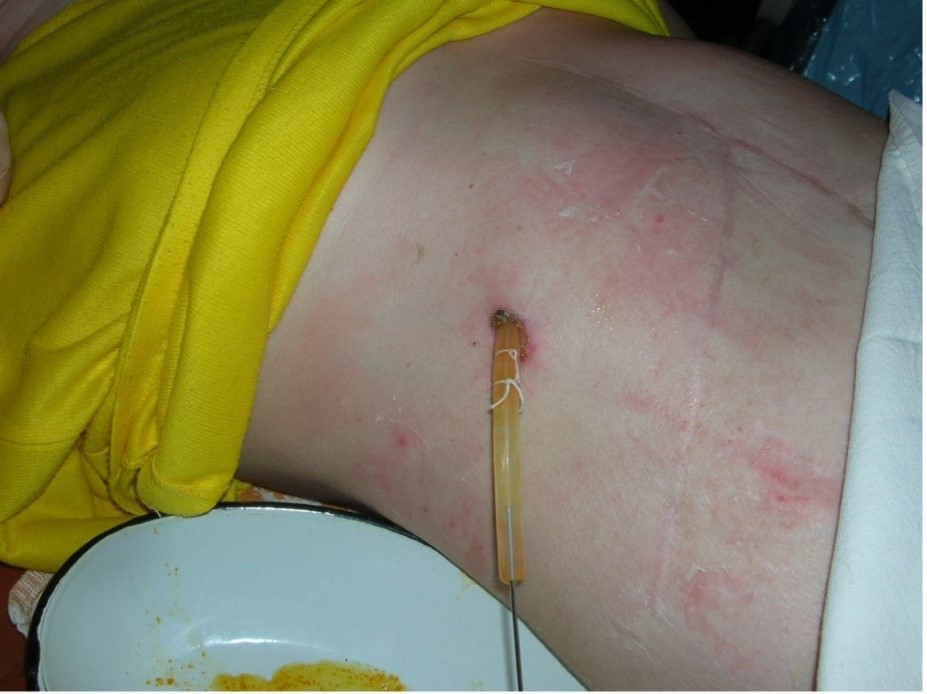
Рис. 3. То же наблюдение. Внешний вид чреспеченочного холангиостомического дренажа большого диаметра
Fig. 3. The same observation. External appearance of a large diameter transhepatic cholangiostomy drainage
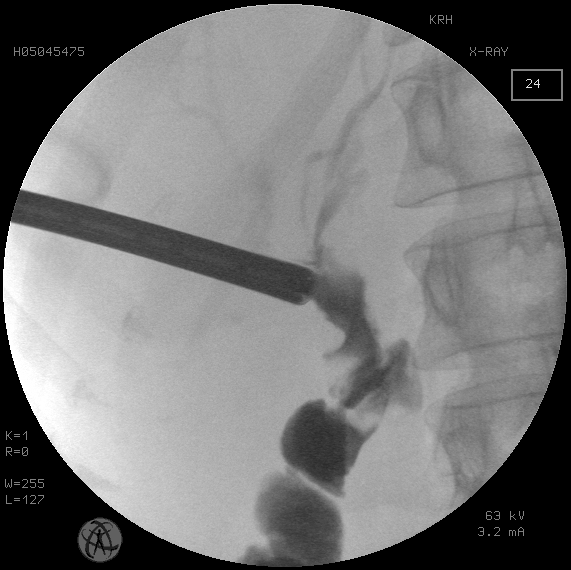
Рис. 4. То же наблюдение. Этапная чрескожная чреспеченочная холелитотрипсия
Fig. 4. The same observation. Staged percutaneous transhepatic cholelithotripsy
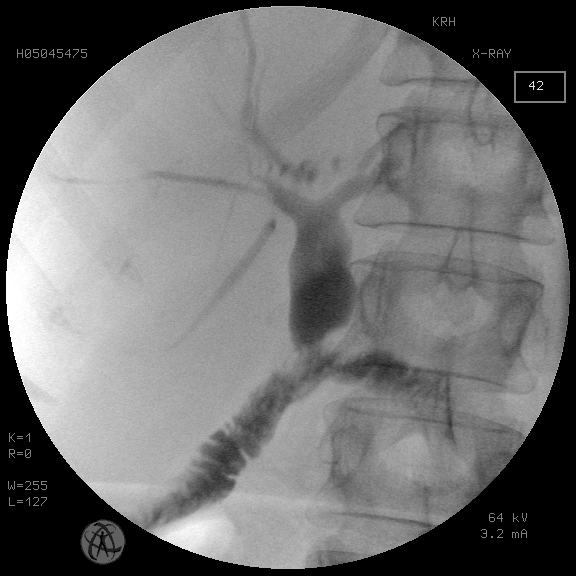
Рис. 5. То же наблюдение. Антеградная холангиография после устранения холелитиаза и стриктуры БДА
Fig. 5. The same observation. Antegrade cholangiography after elimination of cholelithiasis and stricture of the BDA
Результаты исследования
У всех 42 пациентов контрольной группы антеградное рентгенохирургическое вмешательство было эффективным. У пациентов контрольной группы возникли 6 осложнений I–III класса по Clavien – Dindo– 2 незначимые гемобилии, ограниченная поддиафрагмальная гематома и 3 миграции холангиографических дренажей, потребовавших ре-ЧЧХС. У всех больных контрольной группы непосредственный результат рентгенохирургического восстановления проходимости БДА был отличным. Пациентам контрольной группы был реализован протокол рентгенохирургического восстановления проходимости БДА.
При этом у пациентов контрольной группы, которым рентгенохирургическая реконструкция билиодигестивного анастомоза проводилась по классической методике – однократная баллонная дилатация и пролонгированное наружно-внутреннее дренирование не менее 9 месяцев, в течение срока наблюдения (до 5 лет) в 5 случаях (11,9 %) возник рецидив стриктуры, который потребовал повторного рентгенохирургического вмешательства.
Из 42 пациентов контрольной группы в 26 наблюдениях (61,9 %) наружно-внутренний дренаж сохраняли 9 месяцев, в 11 случаях (26,2 %) – 12 месяцев, у 5 пациентов (11,9 %) длительность дренирования составила от 15 до 27 месяцев.
Показатели кумулятивной частоты безрецидивного течения при рентгенохирургической коррекции стриктуры БДА у пациентов без сопутствующего холелитиаза по Каплану – Мейеру представлены на рисунке 6.
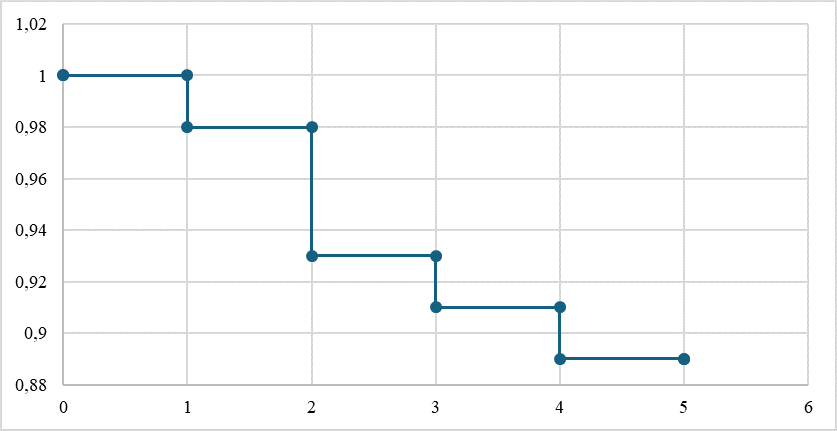
Риc. 6. Частота безрецидивного течения по Каплану – Мейеру у пациентов после рентгенохирургического лечения стриктуры БДА без сопутствующего холелитиаза (наблюдение – 5 лет)
Fig. 6. Frequency of relapse-free course of disease according to Kaplan – Meier in patients after X-ray surgical treatment of stricture of the BDA without concomitant cholelithiasis (observation for 5 years)
В группе исследования у всех 16 пациентов с холелитиазом на фоне стриктуры БДА непосредственный результат использования рентгенохирургических методик был эффективным. Осложнений, связанных с рентгенохирургическим доступом в желчное дерево, а также методиками разрешения холелитиаза, не было. В 12 случаях после однократной баллонной дилатации стриктуры БДА наружно-внутренний дренаж сохраняли 9 месяцев. В 3 случаях баллонная дилатация БДА выполнялась дважды, а дренаж сохраняли 12 месяцев, в одном случае – трижды и наружно-внутренний каркасный дренаж был удален через 15 месяцев после первичного вмешательства.
В 9 наблюдениях (56,3 %) пациентов группы исследования в срок до 5 лет после антеградной реконструкции стриктуры БДА и ликвидации сопряженного с ней холелитиаза возник рецидив стриктуры, потребовавший повторного рентгенохирургического вмешательства.
При оценке достоверности различий в частоте возникновения рецидива стриктуры БДА в группе пациентов с сопутствующим холелитиазом и без него выявлено, что различия достоверны (Х2 с поправкой Йетса 5,351, коэффициент сопряженности Пирсона 0,331, связь прямая, средней силы, p ≤ 0,05). Таким образом, «нулевая гипотеза» отвергается. Имеется прямая достоверная связь средней силы между наличием сопутствующего холелитиаза на фоне стриктуры БДА и частотой 5-летних рецидивов стриктуры после ее рентгенохирургической коррекции.
Показатели кумулятивной частоты безрецидивного течения при рентгенохирургической коррекции стриктуры БДА у пациентов c сопутствующим холелитиазом по Каплану – Мейеру представлены на риcунке 7.
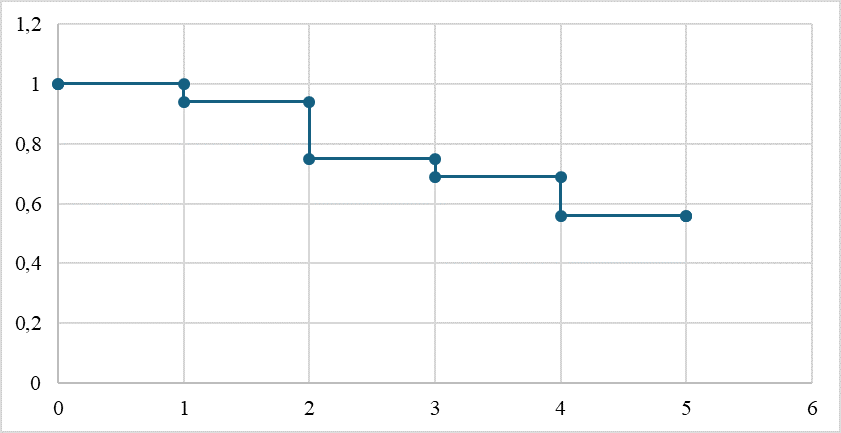
Рис. 7. Частота безрецидивного течения по Каплану – Мейеру у пациентов после рентгенохирургического лечения стриктуры БДА с сопутствующим холелитиазом (наблюдение – 5 лет)
Fig. 7. Frequency of relapse-free course of disease according to Kaplan – Meier in patients after X-ray surgical treatment of stricture of the BDA with concomitant cholelithiasis (observation for 5 years)
Обсуждение
Среди методик лечения рубцовых стриктур БДА приоритетной является рентгенохирургическое чрескожное чреспеченочное вмешательство, последовательно включающее в себя пункционный чрескожный доступ в желчное дерево под лучевым контролем с последующей его модификацией под методику антеградной баллонной дилатации зоны стриктуры с пролонгированным наружно-внутренним билиарным дренированием.
Случаи сочетания рубцовой стриктуры БДА с холелитиазом рассматриваются отдельно. Традиционно холелитиаз, осложняющий стриктуру БДА, рассматривается как фактор, предполагающий хирургическую реконструкцию анастомоза. Тем не менее необходимо отметить, что факт наличия конкрементов проксимальнее зоны БДА еще не является основанием для безусловного отказа от использования рентгенохирургических методик разрешения холелитиаза. Как показали результаты использования антеградного чреспеченочного доступа в желчное дерево с последующей контактной литотрипсией у пациентов группы исследования, полное освобождение желчного дерева от конкрементов было достигнуто у всех больных. При этом использовалась экстремальная модификация первичного холангиостомического доступа до 30 Fr для последующих внутрипротоковых манипуляций с ригидным перкутанным нефроскопом под операционный кожух 24, 26 СН с контактной пневматической литотрипсией (см. рис. 1–5). Такая методика используется нами более 20 лет и зарекомендовала себя не только эффективной, но и безопасной при условии бесконфликтности первичной чреспеченочной пункции желчного дерева [Охотников и др., 2011; Охотников и др., 2012].
Совершенствование как гибких (Spyglass и аналоги), так и жестких (Mini-perc и аналоги) оптических систем прямой визуализации с современными лазерными системами (тулиевый лазер), по-видимому, существенно уменьшат пул пациентов с «трудным» холангиолитиазом, что еще больше минимизирует травматичность вмешательства, риск периоперационных осложнений и общую продолжительность лечения. Кроме того, использование оптических систем, соразмерных с диаметром первичной холангиостомы (8–10 Fr), предполагает возможность рутинного повторения процедуры антеградной литотрипсии в случае рецидива холелитиаза, так же как и проведение рехолангиостомии при рецидиве стриктуры БДА.
С другой стороны, риск рецидива стриктуры в течение 5 лет наблюдения у пациентов с сопутствующим холелитиазом оказался достоверно выше, поэтому дальнейший прогресс в лечении этой сложной категории пациентов будет заключаться не только и не столько в совершенствовании методики литотрипсии, ее рутинной повторяемости и расширении использования за счет пациентов фактически в любом состоянии операбельности, но и в профилактике камнеобразования. Возможно, высокий риск развития стриктуры БДА на фоне холелитиаза свидетельствует о том, что факторы, предрасполагающие к камнеобразованию, обладают потенциирующим влиянием на избыточное развитие и созревание соединительной ткани в зоне БДА, провоцируя формирование стриктуры. Этот предположение нуждается в дополнительном изучении, но делает оправданным использование у таких пациентов в постманипуляционном периоде препаратов, снижающих вязкость и литогенность желчи.
Также интересным представляется отсутствие полной стриктуры БДА на фоне холелитиаза. Механическая желтуха в этом случае обусловлена не полной рубцовой непроходимостью анастомоза, а персистирующим в этой зоне конкрементом, что позволяет даже при множественном холелитиазе уже при первичной пункции внутрипеченочного желчного протока визуализировать зону БДА по сбросу контраста в петлю тонкой кишки или прохождение поискового проводника (рис. 8).
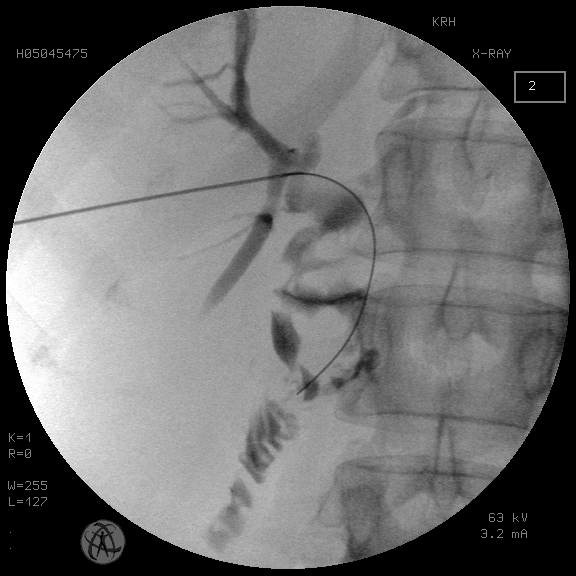
Рис. 8. Прохождение поискового проводника через зону БДА при первичной пункции желчных протоков
Fig. 8. Passage of the search guide through the BDA zone during primary puncture of the bile ducts
Поскольку стриктура БДА на фоне холелитиаза не носит полный характер, то ее антеградная баллонная дилатация не вызывает трудностей, в отличие от «чистой» бескаменной стриктуры, при которой с частотой до 25 % не удается пройти из желчного протока в отводящую петлю тонкой кишки.
Заключение
Антеградное рентгенохирургическое разрешение холелитиаза, сопутствующего рубцовой стриктуре БДА, является эффективным и безопасным способом миниинвазивного лечения этой сложной категории пациентов. Вместе с тем следует иметь в виду, что риск 5-летнего рецидива стриктуры БДА у пациентов с сопутствующим холелитиазом достоверно выше, чем без него, следовательно, такой подход оправдан и практически безальтернативен у больных с некоррегируемо высоким операционно-анестезиологическим риском.





Список литературы
Кулезнева Ю.В., Курмансеитова Л.И., Патрушев И.В., Ефанов М.Г., Цвиркун В.В., Мелехина В.В., Шаповальянц С.Г., Федоров Е.Д., Будзинский С.А., Щеглов В.В., Беляков Р.Ф., Петровский А.Н., Попов А.Ю., Сидоренко А.Б., Багмет Н.Н., Трифонов С.А., Сутягин А.А., Гадаев Ш.Ш., Конысов М.Н., Хистева К.Н., Читадзе А.А., Мусатов А.Б. 2021. Опыт создания базы данных (реестра) больных с посттравматическими рубцовыми билиарными стриктурами. Первые результаты. Анналы хирургической гепатологии, 26(4): 105–113. https://doi.org/10.16931/1995-5464.2021-4-105-113
Ashat M., Berei J., El-Abiad R., Khashab M.A. 2024. Benign Biliary Strictures: A Comprehensive Review. Turk. J. Gastroenterol, 35(7): 513–522. https://doi.org/10.5152/tjg.2024.24044
Chikamori F., Shimizu S., Ito S., Okazaki M., Tanida N., Sharma N. 2022. Percutaneous Stone Removal Using Cobra-Shaped Sheath and Cholangioscopy for Multiple Hepatolithiasis with Choledochoduodenal Anastomotic Stenosis. Radiol Case Rep, 17(6): 1890–1896. https://doi.org/10.1016/j.radcr.2022.03.007
Choi K.K.H., Bonnichsen M., Liu K., Massey S., Staudenmann D., Saxena P., Kaffes A.J. 2023. Outcomes of Patients with Hepaticojejunostomy Anastomotic Strictures Undergoing Endoscopic and Percutaneous Treatment. Endosc. Int. Open, 11(1): E24-E31. https://doi.org/10.1055/a-1952-2135
Colombo M., Forcignanò E., Da Rio L., Spadaccini M., Andreozzi M., Giacchetto C.M., Carrara S., Maselli R., Galtieri P.A., Pellegatta G., Capogreco A., Massimi D., Khalaf K., Hassan C., Anderloni A., Repici A., Fugazza A. 2023. Endoscopic Management of Benign Biliary Strictures: Looking for the Best Stent to Place. World J. Clin. Cases, 11(31): 7521–7529. https://doi.org/10.12998/wjcc.v11.i31.7521
Fan Z., Zhao X., Ji R., Li J., Shi Y. 2022. Endoscopic Treatment of Benign Biliary Stricture Using Different Stents: A Systematic Review and Meta-Analysis. Wideochir. Inne. Tech. Maloinwazyjne, 17(1): 35–60. https://doi.org/10.5114/wiitm.2021.108418
Fang A., Kim I.K., Ukeh I., Etezadi V., Kim H.S. 2021. Percutaneous Management of Benign Biliary Strictures. Semin. Intervent. Radiol., 38(3): 291–299. https://doi.org/10.1055/s-0041-1731087
Giuliante F., Panettieri E., De Rose A. M., Murazio M., Vellone M., Mele C., Clemente G., Giovannini I., Nuzzo G., Ardito F. 2023. Bile Duct Injury After Cholecystectomy: Timing of Surgical Repair Should Be Based on Clinical Presentation. The Experience of a Tertiary Referral Center with Hepp-Couinaud Hepatico-Jejunostomy. Updates in surgery, 75(6): 1509–1517. https://doi.org/10.1007/s13304-023-01611-7
Li T.F., Fu P.J., Han X.W., Ma J., Zhu M., Li Z., Ren J.Z. 2020. Repeated Balloon Dilatation with Long-Term Biliary Drainage for Treatment of Benign Biliary-Enteric Anastomosis Strictures: A STROBE-Compliant Article. Medicine (Baltimore), 99(44): e22741. https://doi.org/10.1097/MD.0000000000022741
Mie T., Sasaki T., Okamoto T., Takeda T., Mori C., Yamada Y., Furukawa T., Kasuga A., Matsuyama M., Ozaka M., Sasahira N. 2024. Risk Factors for Recurrent Stenosis After Balloon Dilation for Benign Hepaticojejunostomy Anastomotic Stricture. Clin. Endosc., 57(2): 253–262. https://doi.org/10.5946/ce.2022.216
Nagai K., Mukai S., Abe M., Sofuni A., Tsuchiya T., Tanaka R., Tonozuka R., Yamamoto K., Matsunami Y., Kojima H., Minami H., Asano K., Itoi T. 2024. Long-Term Outcomes After EUS-guided Antegrade Intervention for Benign Bilioenteric Anastomotic Stricture. Gastrointest. Endosc., 99(1): 50–60. https://doi.org/10.1016/j.gie.2023.07.052
Nagakawa Y., Kozono S., Takishita C., Osakabe H., Nishino H., Nakagawa N., Suzuki K., Hayashi Y., Ishizaki T., Katsumata K., Tsuchida A. 2021. Incidence of Anastomotic Stricture After Hepaticojejunostomy with Continuous Sutures in Patients who Underwent Laparoscopic Pancreaticoduodenectomy. Surg Today, 51(7): 1212–1219. https://doi.org/10.1007/s00595-020-02223-z
Nunes T.F., Inchingolo R., Morais N.R., Tibana T.K., Fornazari V.A.V., da Motta-Leal-Filho J.M., Spiliopoulos S. 2022. Long-Term Results of Oversized Balloon Dilation for Benign Anastomotic Biliary Strictures: Initial Two-Center Experience. Radiol. Bras., 55(2): 90–96. https://doi.org/10.1590/0100-3984.2021.0027
Raafat M., Morsy M.M., Mohamed S.I., Hamad M.A., Sayed M.M. 2023. Hepaticojejunostomy with Gastric Access Loop Versus Conventional Hepaticojejunostomy: A Randomized Trial. Updates Surg., 75(8): 2157–2167. https://doi.org/10.1007/s13304-023-01604-6
Sato T., Kogure H., Nakai Y., Kanai S., Ishigaki K.., Hakuta R., Saito K., Saito T., Takahara N., Hamada T., Mizuno S., Yamada A., Isayama H., Koike K. 2021. Endoscopic Treatment of Hepaticojejunostomy Anastomotic Strictures Using Fully-Covered Metal Stents. Dig. Endosc, 33(3): 451–457. https://doi.org/10.1111/den.13773
Sato T., Nakai Y., Fujishiro M. 2022. Current Endoscopic Approaches to Biliary Strictures. Curr. Opin. Gastroenterol, 38(5): 450–460. https://doi.org/10.1097/MOG.0000000000000857
Schreuder A.M., Busch O.R., Besselink M.G., Ignatavicius P., Gulbinas A., Barauskas G., Gouma D.J. van Gulik T.M. 2020. Long-Term Impact of Iatrogenic Bile Duct Injury. Digestive surgery, 37(1): 10–21. https://doi.org/10.1159/000496432
Suzuki Y., Yoshida M., Fujisawa T., Shimatani M., Tsuyuguchi T., Mori T., Tazuma S., Isayama H., Tanaka A. 2024. Assessing Outcomes and Complications of Secondary Hepatolithiasis After Choledochoenterostomy: A Nationwide Survey in Japan. J. Hepatobiliary Pancreat. Sci., 31(10): 716–725. https://doi.org/10.1002/jhbp.12061
Ye P., Zeng Q., Miao H., Pang H., Chen Y. 2021. Percutaneous Treatment of Benign Biliary Anastomotic Strictures: Retrievable Covered Self-Expandable Metal Stent with Fixation String Versus Large-Bore Catheters. J. Vasc. Interv. Radiol., 32(1): 113–120. https://doi.org/10.1016/j.jvir.2020.01.034
Yung K. K., Jin Y. C., Hwan L. J., Lee C.H. 2024. Percutaneous Treatment of Bilioenteric Anastomotic Strictures: Comparison of Long-Term Outcomes Between Temporary Covered Stents and Balloon Dilation. Eur. J. Radiol., 181: 111816. https://doi.org/10.1016/j.ejrad.2024.111816