Инфекционные осложнения после плановых операций в многопрофильном стационаре
Aннотация
В исследование включено 326 пациентов, которые находились на лечении в отделении хирургических инфекций Белгородской областной клинической больницы Святителя Иоасафа с гнойными послеоперационными ранами в период с 2018 по 2022 год после выполнения им плановых операций. Наибольшее число госпитализированных нами больных с нагноением послеоперационной раны были ранее прооперированы по поводу грыж – 116 (35,58 %), на втором месте по количеству была группа пациентов после операций на органах брюшной полости (лапаротомия) – 50 (15,34 %), больных с инфекцией кожи и мягких тканей после операций на костной ткани (металлоостеосинтез) было 32 (9,82 %), после (тотального эндопротезирования крупных суставов) – 48 (14,72 %) пациентов, операции на периферических сосудах нижних конечностей были выполнены у 50 (15,34 %) пациентов, у 30 (9,2 %) пациентов ранее были выполнены операции на органах средостения (стернотомия). Из общего перечня возможных причин развития гнойных раневых осложнений после плановых оперативных вмешательств, описанных в литературе, нами была выявлена частота их встречаемости, а корреляционный анализ позволил выделить те из них, которые имели наиболее тесную связь с результирующим показателем (факт нагноения раны после операции с ранжированием степени тяжести гнойно-воспалительного процесса по шкале ASEPSIS). Построенные на основе выявленных параметров регрессионные модели характеризовались высокими коэффициентами детерминации (> 0,8), являлись значимыми (достоверными) и позволили прогнозировать ожидаемое значение оценки послеоперационной раны пациента. Установлено, что достоверными предикторами развития гнойных раневых осложнений у больных после плановых операций являются использование синтетических и металлических имплантов, температура в операционном помещении < 21 С или > 24 С, площадь раны, см2 и наличие гематомы мягких тканей в области послеоперационной раны.
Ключевые слова: предикторы гнойных осложнений, плановая операция, матрица парных корреляций факторов
Введение
В настоящее время раневая хирургическая инфекция является одной из основных проблем, с которыми больные обращаются за хирургической помощью [Arsalan-Werner et al., 2020; Goswami, 2020; Payá-Llorente et al., 2020; Pinto et al., 2020; Boussion et al., 2021]. Сложность данной проблемы определяется и тем, что 16,0 % от всех внутрибольничных инфекций составляют послеоперационные раневые осложнения [Алешина, 2019; СанПиН, 2021; Boussion et al., 2021; Póvoa et al., 2021]. Современные мультицентровые исследования показывают, что частота нагноения ран после оперативных вмешательств может достигать 27,0 %, достоверно увеличиваясь при наличии определенных факторов риска [Зубрицкий и др., 2021; Pan et al., 2021; Di Franco et al., 2022; Shukla et al., 2022].
Принято выделять экзогенные и эндогенные факторы риска. К первым относят повреждения кожных покровов, несоблюдение гигиенических правил, перегревание и переохлаждение. Ко вторым – нарушения в системе иммунитета врожденного или приобретенного генеза, изменения нутритивного статуса, сопутствующие заболевания, эндокринные расстройства и т. д. [Алешина, 2019; Князев и др., 2022; Arulkumaran et al. 2020; Gierek et al., 2022]. Кроме того, факторы риска могут быть модифицируемые (курение, нарушение нутритивного статуса) и немодифицируемые (возраст, онкологические заболевания). Многие факторы риска могут быть нивелированы во время подготовки к плановому оперативному вмешательству (отказ от курения, устранение нутритивных нарушений и т. д.), в то время как при ургентной ситуации времени на их устранение не остается [Киреева и др., 2021; Шулакова и др., 2021; Guzin et al., 2021; Oppelt et al., 2021; Di Franco et al., 2022].
Цель исследования: на основании ретроспективных данных провести анализ причин гнойных раневых осложнений у больных после плановых операций и выявить наиболее достоверные прогностические факторы риска их развития.
Объект и методы исследования
В исследование включено 326 пациентов, которые находились на лечении в отделении хирургических инфекций Белгородской областной клинической больницы Святителя Иоасафа с гнойными послеоперационными ранами в период с 2018 по 2022 год после выполнения им плановых операций.
Срок поступления больных с момента выполнения им оперативных вмешательств варьировал от 5 дней до 30 дней.
Наибольшее число госпитализированных нами больных с нагноением послеоперационной раны были ранее прооперированы по поводу грыж – 116 (35,58 %). При этом вентральные послеоперационные грыжи были у 80 (24,54 %), паховые – у 21 (6,44 %), пупочные – у 15 (4,6 %). Было выполнено 2 вида операций: пластика с применением сетчатых имплантов – 102 (31,29 %) и пластика местными тканями – 14 (4,29 %).
На втором месте по количеству была группа пациентов после операций на органах брюшной полости (лапаротомия) – 50 (15,34 %), при этом реконструктивные операции на желчных протоках были выполнены у 28 (8,59 %), резекция печени – у 10 (3,07 %), панкреатодуоденальная резекция – у 10 (3,07 %), резекция участка кишки по поводу опухоли – у 2 (0,61 %).
Больных с инфекцией кожи и мягких тканей после операции на костях (металлоостеосинтез) было 32 (9,82 %), после (тотального эндопротезирования крупных суставов) – 48 (14,72 %) пациентов. При этом эндопротезирование тазобедренного сустава было выполнено у 35 (10,74 %), коленного сустава – у 13 (3,99 %).
Операции на периферических сосудах нижних конечностей были ранее выполнены у 50 (15,34 %) пациентов, при этом аорто-бедренное шунтирование – у 27 (8,28 %), подвздошно-бедренное шунтирование – у 13 (3,99 %) и бедренно-подколенное шунтирование – у 10 (3,7 %).
У 30 (9,2 %) пациентов с инфекцией кожи и мягких тканей послеоперационной раны ранее были выполнены операции на органах средостения (стернотомия).
С целью сравнения и определения степени тяжести гнойного воспалительного процесса в послеоперационной ране нами была использована шкала ASEPSIS (табл. 1).
Таблица 1
Table 1
Шкала оценки операционной раны ASEPSIS
ASEPSIS wound score
Характеристика раны | Участок раны, вовлеченный в воспаление ( %) | ||||
< 20 | 20–39 | 40–59 | 60–79 | > 80 | |
Серозные выделения | 1 | 2 | 3 | 4 | 5 |
Эритема | 1 | 2 | 3 | 4 | 5 |
Гнойные выделения | 2 | 4 | 6 | 8 | 10 |
Расхождение глубоких слоев раны | 2 | 4 | 6 | 8 | 10 |
Дополнительные баллы | |||||
Антибиотикотерапия | 10 |
| |||
Дополнительное рассечение или дренирование | 5 | ||||
Хирургическая обработка | 10 | ||||
Лабораторное подтверждение путем выделения бактерий | 10 | ||||
Госпитализация более 14 дней | 5 | ||||
Необходимость в амбулаторной лечении | 5 | ||||
Интерпретация результатов | |||||
Общее количество баллов | Категория заживления раны | ||||
0–10 | удовлетворительное заживление | ||||
11–20 | нарушенное заживление | ||||
21–30 | минимальное инфицирование | ||||
31–40 | умеренное инфицирование | ||||
> 40 | тяжелая раневая инфекция | ||||
В качестве возможных причин развития гнойных раневых осложнений у больных после плановых операций, описанных в литературе, нами была проанализирована встречаемость следующих признаков [СанПиН, 2021; Boussion et al., 2021; Guzin et al., 2021; Póvoa et al., 2021; Gierek et al., 2022]:
- возраст пациента старше 60 лет;
- наличие сахарного диабета;
- площадь раны, см2;
- алиментарно-конституциональное ожирение;
- толщина подкожно-жировой клетчатки более 3 см;
- оперативный доступ с рассечением костной ткани;
- использование синтетических и металлических имплантов (сетка, сустав, проволока, шунт, стент и др.);
- обширная сепарация тканей;
- объем кровопотери во время операции больше 400 мл;
- установка дренажной трубки через рану;
- обработка рук хирургической бригады первомуром;
- обработка операционного поля по Филончикову – Гроссиху;
- замена перчаток при повреждении во время операции;
- температура в операционном помещении < 21 °С или > 24 °С;
- длительность оперативного вмешательства > 4 часов;
- вскрытие полого органа во время операции;
- наличие выпота в брюшной полости;
- дополнительное расширение хирургического доступа;
- температура воздуха в палате > 24 °С;
- использование многоразового операционного белья;
- использование электроинструмента при рассечении кожи и подкожно-жировой клетчатки;
- использование нерассасывающегося шовного материала при закрытии дефекта мягких тканей;
- установка перчаточного выпускника через рану;
- наличие гематомы мягких тканей в области послеоперационной раны;
- наличие серомы мягких тканей в области послеоперационной раны;
- ежедневное выполнение перевязки.
С целью выявления наиболее достоверных факторов риска развития гнойных осложнений со стороны послеоперационной раны использовали корреляционный и многомерный регрессионный анализы с последующим сравнением фактических величин интегральной оценки операционной раны и величин, рассчитанных с использованием регрессионных моделей. С использованием прикладного пакета статистического анализа данных Statistica 12 pro по данным общей базы данных составлена матрица парных корреляций факторов с результирующим показателем.
Результаты исследования
Первоначально мы проанализировали частоту выявления исследованных факторов у больных после плановых оперативных вмешательств (табл. 2). Далее нами была составлена матрица парных корреляций факторов с результирующим показателем (степень тяжести гнойного воспалительного процесса по шкале ASEPSIS) (табл. 3). В таблице представлены факторы, имеющие наиболее тесную связь с результирующим показателем (жирный), а также факторы (курсив), связь которых характеризуется значением коэффициента R на границе достоверности.
Таблица 2
Table 2
Частота выявления факторов развития гнойных раневых осложнений у больных после плановых операций
Frequency of detection factors of the development of purulent wound complications in patients after planned surgery
Фактор | Операции по поводу грыж (116 чел.) | Операции на органах брюшной полости (лапаротомия) (50 чел.) | Операции на костной ткани (тотальное эндопротезирование крупных суставов) (48 чел.) | Операции на костной ткани (металл-остеосинтез) (32 чел.) | Операции на периферических сосудах нижних конечностей | Операции на органах средостения (стернотомия) (30 чел.) |
1 | 2 | 3 | 4 | 5 | 6 | 7 |
Возраст пациента старше 60 лет | 44 (37,93 %) | 20 (50 %) | 11 (55 %) | 25 (78,12 %) | 19 (76 %) | 13 (52 %) |
Наличие сахарного диабета | 69 (59,48 %) | 22 (55 %) | 8 (40 %) | 20 (62,5 %) | 16 (64 %) | 12 (48 %) |
Площадь раны, см2 | 73 (62,93 %) | 31 (77,5 %) | 7 (35 %) | 21 (65,62 %) | 21 (84 %) | 15 (60 %) |
Алиментарно-конституциональное ожирение | 71 (61,21 %) | 21 (52,5 %) | 4 (20 %) | 24 (75 %) | 18 (72 %) | 10 (40 %) |
Толщина подкожно-жировой клет-чатки в зоне разреза более 3 см | 70 (60,34 %) | 19 (47,5 %) | 9 (45 %) | 21 (65,62 %) | 13 (52 %) | 3 (12 %) |
Использование синтетических и металлических имплантов | 97 (83,62 %) | 15 (58 %) | 20 (100 %) | 32 (100 %) | 25 (100 %) | 17 (68 %) |
Обширная сепарация мягких тканей | 70 (60,34 %) | 21 (52,5 %) | 19 (95 %) | 27 (84,37 %) | 20 (80 %) | 13 (52 %) |
Объем кровопотери во время операции больше 400 мл | 9 (7,76 %) | 16 (40 %) | 9 (45 %) | 10 (31,25 %) | 13 (52 %) | 16 (64 %) |
Установка дренажной трубки «через рану» | 54 (46,55 %) | 17 (42,5 %) | 11 (55 %) | 9 (28,12 %) | 14 (56 %) | 11 (44 %) |
Обработка рук хирургической бригады первомуром | 58 (50 %) | 18 (45 %) | 12 (60 %) | 12 (37,5 %) | 16 (64 %) | 14 (56 %) |
Обработка операционного поля по Филончикову – Гроссиху | 26 (22,41 %) | 4 (10 %) | 4 (20 %) | 5 (15,62 %) | 9 (36 %) | 7 (28 %) |
Замена обеих перчаток при повреждении во время операции | 12 (10,34 %) | 13 (32,5 %) | 8 (40 %) | 7 (21,87 %) | 6 (24 %) | 8 (32 %) |
Температура в операционном помещении < 21 ºС или > 24 ºС | 78 (67,24 %) | 29 (72,5 %) | 16 (80 %) | 15 (46,87 %) | 18 (72 %) | 2 (8 %) |
Длительность оперативного вмешательства > 4 часов | 39 (33,69 %) | 22 (55 %) | 13 (65 %) | 6 (18,75 %) | 15 (60 %) | 16 (64 %) |
Вскрытие полого органа во время операции | 1 (0,86 %) | 8 (20 %) | – | – | – | – |
Наличие выпота в брюшной полости | 24 (20,69 %) | 29 (72,5 %) | – | – | – | – |
Дополнительное расширение хирургического доступа во время операции | 82 (70,69 %) | 32 (80 %) | 9 (45 %) | 18 (56,25 %) | 21 (84 %) | 10 (40 %) |
Использование многоразового операционного белья | 73 (62,93 %) | 29 (72,5 %) | 9 (45 %) | 17 (53,12 %) | 17 (68 %) | 2 (8 %) |
Использование нерассасывающегося шовного материала при закрытии дефекта мягких тканей | 89 (76,72 %) | 35 (87,5 %) | 14 (70 %) | 26 (81,25 %) | 19 (76 %) | 17 (68 %) |
Установка перчаточного выпускника «в рану» | 86 (74,14 %) | 33 (82,5 %) | 10 (50 %) | 19 (59,37 %) | 13 (52 %) | 17 (68 %) |
Наличие гематомы мягких тканей в области послеоперационной раны | 17 (14,66 %) | 7 (17,5 %) | 2 (10 %) | 20 (62,5 %) | 9 (36 %) | 4 (16 %) |
Наличие серомы мягких тканей в области послеоперационной раны | 64 (55,17 %) | 26 (65 %) | 9 (45 %) | 12 (37,5 %) | 11 (44 %) | 11 (44 %) |
Ежедневное выполнение перевязок | 72 (62,07 %) | 9 (20 %) | 17 (85 %) | 18 (56,25 %) | 20 (80 %) | 13 (52 %) |
Таблица 3
Table 3
Значения коэффициентов корреляции R факторов с результирующим признаком (интегральной оценкой раны) для групп больных после плановых операций
Values of correlation coefficients of R factors with the resulting characteristics (integrated wound assessment) for groups of patients after planned surgery
Группа больных Фактор | Операции по поводу грыж | Операции на органах брюшной полости (лапаротомия | Операции на костной ткани (тотальное эндопротезирование крупных суставов | Операции на костной ткани (металлостеосинтез | Операции на периферических сосудах нижних конечностей | Операции на органах средостения (стернотомия |
Возраст пациента старше 60 лет | -0,11 | -0,05 | -0,29 | 0,17 | -0,24 | 0,09 |
Наличие сахаренного диабета | 0,64 | 0,71 | 0,77 | 0,68 | 0,74 | 0,67 |
Площадь раны, см2 | 0,87 | 0,71 | 0,63 | 0,87 | 0,71 | 0,84 |
Алиментарно-конституциональное ожирение | 0,07 | 0,09 | 0,05 | 0,09 | 0,09 | -0,08 |
Толщина подкожно-жировой клетчатки более 3 см | 0,64 | 0,65 | 0,61 | 0,71 | 0,65 | 0,42 |
Оперативный доступ с рассечением костной ткани | 0,00 | 0,00 | -0,11 | 0,31 | 0,00 | 0,46 |
Использование синтетических и металлических имплантов | 0,72 | 0,00 | 0,30 | 0,93 | 0,36 | 0,97 |
Обширная сепарация тканей | 0,05 | 0,06 | -0,07 | 0,12 | 0,00 | 0,10 |
Объем кровопотери во время операции больше 400 мл | -0,19 | 0,10 | 0,16 | 0,06 | 0,10 | 0,09 |
Установка дренажной трубки через рану | 0,26 | 0,37 | 0,45 | 0,34 | 0,48 | 0,00 |
Обработка рук хирургической бригады первомуром | -0,22 | -0,27 | -0,23 | -0,19 | -0,29 | -0,25 |
Обработка операционного поля по Филончикову – Гроссиху | 0,15 | 0,23 | 0,16 | 0,13 | 0,27 | 0,09 |
Замена перчаток при повреждении во время операции | -0,02 | 0,29 | 0,09 | 0,26 | 0,25 | 0,01 |
Температура в операционном помещении < 21 ºС или > 24 ºС | 0,95 | 0,92 | 0,91 | 0,97 | 0,92 | 0,89 |
Длительность оперативного вмешательства > 4 часов | 0,33 | 0,06 | 0,00 | 0,34 | 0,06 | 0,38 |
Вскрытие полого органа во время операции | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
Наличие выпота в брюшной полости | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
Дополнительное расширение хирургического доступа | 0,09 | 0,14 | 0,17 | 0,09 | 0,19 | 0,18 |
Температура воздуха в палате > 24 ºС | 0,87 | 0,74 | 0,71 | 0,93 | 0,74 | 0,78 |
Использование многоразового операционного белья | -0,14 | 0,20 | -0,19 | 0,02 | 0,21 |
|
Использование электроинструмента при рассечении кожи и подкожно-жировой клетчатки | 0,39 | 0,29 | 0,71 | 0,61 | 0,47 | 0,56 |
Использование нерассасывающегося шовного материала при закрытии дефекта мягких тканей | 0,01 | 0,28 | 0,49 | 0,08 | 0,41 | 0,51 |
Установка перчаточного выпускника через рану | 0,34 | 0,50 | 0,47 | 0,34 | 0,72 |
|
Наличие гематомы мягких тканей в области послеоперационной раны | 0,84 | 0,74 | 0,71 | 0,88 | 0,74 | 0,34 |
Наличие серомы мягких тканей в области послеоперационной раны | -0,01 | 0,22 | 0,21 | 0,05 | 0,22 | 0,11 |
Ежедневное выполнение перевязки | 0,10 | 0,04 | 0,30 | 0,09 | 0,42 | 0,02 |
По результатам анализа оценки взаимосвязи исследуемых признаков установлено, что наиболее тесно связаны с результирующим показателем следующие факторы:
- температура в операционном помещении <21 ºС или >24 ºС;
- температура воздуха в палате > 24 ºС;
- использование синтетических и металлических имплантов;
- площадь раны, см2;
- наличие гематомы мягких тканей в области послеоперационной раны;
- наличие сахарного диабета;
- толщина подкожно-жировой клетчатки более 3 см;
- использование электроинструмента при рассечении кожи и подкожно-жировой клетчатки;
- использование нерассасывающегося шовного материала при закрытии дефекта мягких тканей.
Факторы «Наличие гематомы мягких тканей в области послеоперационной раны»
и «Толщина подкожно-жировой клетчатки более 3 см» значимы для всех операций,
кроме операций на органах средостения. Для операций на органах средостении
наиболее значимым фактором является «Использование синтетических и металлических имплантов».
Связь с результатом таких показателей, как «Установка перчаточного выпускника через рану», «Установка дренажной трубки через рану», «Длительность оперативного вмешательства > 4 часов», «Оперативный доступ с рассечением костной ткани», характеризуется величиной коэффициентов корреляции, находящихся на границе достоверности, поэтому их можно считать вторичными.
Степень связи остальных факторов характеризуется значениями коэффициентов корреляции, выходящих за диапазон достоверных значений, и для формирования уверенного вывода о наличии и характере этой связи необходимо кратно увеличивать количество наблюдений.
Поскольку значения коэффициентов корреляции характеризуют наличие и тесноту парной связи, а влияние на результат имеет комплексный (многофакторный) характер, для более точной оценки степени влияния показателей на результат необходимо проведение многомерного регрессионного анализа.
Для возможности формирования вывода о значимости признаков на основании регрессионных коэффициентов значения семи основных оказывающих на результат факторов были пронормированы в рамках диапазона [0, 1]. Построены линейные регрессионные модели (по всем исследованным группам больных). Аналитический вид регрессионной модели имеет вид:
R = A0 + A1 ∙ F1 + A2 ∙ F2 + A3 ∙ F3 + A4 ∙ F4 + A5 ∙ F5 + A6 ∙ F6 + A7 ∙ F7
где Fi – факторы и Аi – коэффициенты в регрессионной модели (табл. 4).
Все сформированные регрессионные модели значимы по критерию
Фишера (F-критерий намного меньше 0,05), а близость величины нормированного коэффициента детерминации (нормированный R-квадрат) к единице говорит
о том, что точность прогноза с использованием такой модели будет достаточно
высокая.
Таблица 4
Table 4
Значения регрессионных коэффициентов факторов (нормированных в рамках диапазона [0, 1]) для групп больных после плановых операций
Values of regression coefficients of factors (normalized within the range [0, 1]) for groups of patients after planned surgery
Фактор | Коэффициент в регрессионной модели |
1 | 2 |
Операции по поводу грыж (116 чел.) | |
Температура в операционном помещении < 21°С или > 24 °С | 13,99 |
Площадь раны, см2 | 8,54 |
Наличие гематомы мягких тканей в области послеоперационной раны | 7,13 |
Температура воздуха в палате > 24 °С | 4,21 |
Толщина подкожно-жировой клетчатки более 3 см | 3,23 |
Наличие сахарного диабета | 1,31 |
Использование синтетических и металлических имплантов | 0,34 |
Операции на органах брюшной полости (лапаротомия) (50 чел.) | |
Температура в операционном помещении < 21°С или > 24 °С | 14,28 |
Температура воздуха в палате > 24 °С | 12,39 |
Наличие гематомы мягких тканей в области послеоперационной раны | 7,36 |
Толщина подкожно-жировой клетчатки более 3 см | 4,02 |
Наличие сахарного диабета | 1,65 |
Площадь раны, см2 | 0,51 |
Использование электроинструмента при рассечении кожи и подкожно-жировой клетчатки | 0,01 |
Операции на костной ткани (тотальное эндопротезирование крупных суставов) (48 чел.) | |
Температура в операционном помещении < 21 °С или > 24 °С | 3,50 |
Наличие сахарного диабета | 1,31 |
Наличие гематомы мягких тканей в области послеоперационной раны | 0,51 |
Толщина подкожно-жировой клетчатки более 3 см | 0,40 |
Использование синтетических и металлических имплантов | 0,34 |
Площадь раны, см2 | 0,19 |
Температура воздуха в палате > 24 °С | 0,15 |
Операции на костной ткани (металлостеосинтез) (32 чел.) | |
Использование синтетических и металлических имплантов | 12,79 |
Температура в операционном помещении < 21 °С или > 24 °С | 11,11 |
Площадь раны, см2 | 7,48 |
Температура воздуха в палате > 24 °С | 6,15 |
Наличие гематомы мягких тканей в области послеоперационной раны | 5,12 |
Толщина подкожно-жировой клетчатки более 3 см | 2,44 |
Наличие сахарного диабета | 1,37 |
Операции на периферических сосудах нижних конечностей (50 чел.) | |
Температура воздуха в палате > 24 °С | 16,40 |
Температура в операционном помещении < 21°С или > 24 °С | 14,23 |
Наличие гематомы мягких тканей в области послеоперационной раны | 8,54 |
Толщина подкожно-жировой клетчатки более 3 см | 4,16 |
Площадь раны, см2 | 1,54 |
Использование электроинструмента при рассечении кожи и подкожно-жировой клетчатки | 0,97 |
Наличие сахарного диабета | 0,30 |
Операции на органах средостения (стернотомия) (30 чел.) | |
Наличие сахарного диабета | 0,63 |
Площадь раны, см2 | 5,59 |
Использование синтетических и металлических имплантов | 23,23 |
Температура в операционном помещении < 21°С или > 24 °С | 5,38 |
Температура воздуха в палате > 24 °С | 13,19 |
Использование электроинструмента при рассечении кожи и подкожно-жировой клетчатки | 1,11 |
Использование нерассасывающегося шовного материала при закрытии дефекта мягких тканей | 1,15 |
Приведенные в таблице значения коэффициентов регрессионной модели позволяют сделать вывод о степени влияния изменения факторов на изменение результата (при одинаковом относительном изменении факторов).
Видно, что практически для всех групп больных на изменение величины интегральной оценки операционной раны наибольшее влияние оказывают изменения таких показателей, как:
- использование синтетических и металлических имплантов;
- температура в операционном помещении <21 ºС или > 24 ºС;
- площадь раны, см2;
- температура воздуха в палате >24 ºС.
Наименьшее значение регрессионного коэффициента перед значением фактора «Наличие сахарного диабета» связано в первую очередь с его бинарным представлением – очевидно, что, если бы имелась возможность его представления более широким спектром численных значений, регрессионный коэффициент в модели бы вырос.
На последнем этапе исследования были построены регрессионные модели с использованием изначальных данных (без их нормировки). Показатели качества данных моделей не отличаются от предыдущих, так как фактически используется та же база данных.
Сравнение фактических величин интегральной оценки операционной раны и величин, рассчитанных с использованием регрессионных моделей, показывают хорошее совпадение реальных и прогнозных значений, что подтверждает ранее сделанные выводы о хорошем качестве сформированных регрессионных зависимостей.
На рисунках 1–6 приведены графики фактической и прогнозной оценки состояния операционной раны исследованных пациентов, визуализирующие хорошее качество сформированных моделей.

Рис. 1. График изменений фактической и прогнозной оценки операционной раны для группы больных после операций по поводу грыжесечения
Fig. 1. Graph of changes of actual and predicted surgical wound assessment for the group of patients after hernia repair
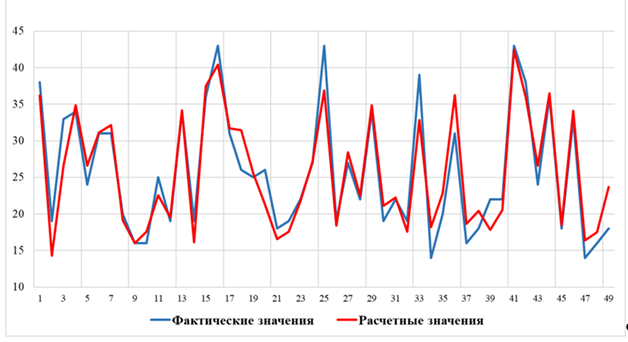
Рис. 2. График изменений фактической и прогнозной оценки операционной раны для группы больных после операций на органах брюшной полости – лапаротомия
Fig. 2. Graph of changes of actual and predicted surgical wound assessment for the group of patients after abdominal surgery – laparotomy

Рис. 3. График изменений фактической и прогнозной оценки операционной раны для группы больных после операций на костной ткани (тотальное эндопротезирование крупных суставов)
Fig. 3. Graph of changes of actual and predicted surgical wound assessment for the group of patients after bone surgery (total endoprosthesis of large joints)

Рис. 4. График изменений фактической и прогнозной оценки операционной раны для группы больных после операций на костной ткани (установка металлостеосинтеза)
Fig. 4. Graph of changes of actual and predicted surgical wound assessment for the group of patients after bone surgery (osteosynthesis installation)

Рис. 5. График изменений фактической и прогнозной оценки операционной раны для группы больных после операций на периферических сосудах нижних конечностей
Fig. 5. Graph of changes of actual and predicted surgical wound assessment for the group of patients after operations peripheral vessels of the lower extrimities

Рис. 6. График изменений фактической и прогнозной оценки операционной раны для группы больных после операций на органах средостения (стернотомия)
Fig. 6. Graph of changes of actual and predicted surgical wound assessment for the group of patients after surgery on the mediastinum organs (sternotomy)
Обсуждение
К сегодняшнему дню описаны многочисленные факторы риска, имеющие определенный вклад в процесс развития инфекции в области послеоперационной раны, и предложено множество рекомендаций по ее профилактике [Arsalan-Werner et al., 2020; Nita et al., 2021; Neupane et al., 2022]. Несмотря на значительные успехи в изучении причин развития гнойных послеоперационных осложнений, большинство исследований современных авторов достаточно противоречивы и не имеют сильной доказательной базы. До конца нерешенными остаются вопросы влияния на развитие инфекции в послеоперационной ране таких факторов, как обработка кожи области разреза от центра до периферии (по Филончикову – Гроссиху), проведение операции с использованием синтетических и металлических имплантов в операционной с ультрачистым воздухом, использование одноразового или сменного (после неоднократной стирки) операционного костюма и операционного белья, ежедневые смены повязки с учётом правил асептики в послеоперационном периоде, выбор антисептика и оптимальное время обработки рук хирурга перед операцией, температура в помещении операционной и перевязочной и др. [Российские Национальные рекомендации, 2019; Boussion et al., 2021; Pörner et al., 2021].
На решение этих и других вопросов и были направлены наши исследования. Из общей базы данных возможных причин развития гнойных раневых осложнений после плановых оперативных вмешательств нами была выявлена частота их встречаемости в различных группах больных, а корреляционный анализ позволил выделить те из них, которые имели наиболее тесную связь с результирующим показателем (факт нагноения раны после операции с ранжированием степени тяжести гнойно-воспалительного процесса по шкале ASEPIS): «температура в операционном помещении < 21 ºС или > 24 ºС», «температура воздуха в палате > 24 ºС», «использование синтетических и металлических имплантов», «площадь раны в см2», «наличие гематомы мягких тканей в области послеоперационной раны», «наличие сахарного диабета», «толщина подкожно-жировой клетчатки более 3 см». Влияние этих факторов характеризовалось прямой связью. Также значимая и достаточно сильная связь была выявлена у фактора «использование электроинструмента при рассечении кожи и подкожно-жировой клетчатки», который может быть отнесен как к группе максимально влияющих, так и к группе вторичных факторов (для разных типов операций), то есть факторов с результатом на границе достоверности.
С использованием семи наиболее тесно связанных с результатом (факт нагноения раны после операции с ранжированием степени тяжести гнойно-воспалительного процесса по шкале ASEPSIS) параметров нами были построены регрессионные модели, которые характеризовались высокими коэффициентами детерминации (> 0,8), являлись значимыми (достоверными) и позволили прогнозировать ожидаемое значение оценки послеоперационной раны пациента. Установлено, что наиболее сильно на динамику изменения состояния послеоперационной раны оказывали такие показатели, как «использование синтетических и металлических имплантов», «температура в операционном помещении < 21 ºС или > 24 ºС», «площадь раны в см2», «наличие гематомы мягких тканей в области послеоперационной раны». Регрессионные коэффициенты этих показателей являлись уверенно значимыми. Построенные графики фактических и рассчитанных по модели значений оценки послеоперационной раны подтвердили уровень качества сформированных моделей, позволяющий применять их в качестве прогнозного инструмента и верифицирующий ранее сделанные выводы.
Таким образом, полученные результаты позволили выявить достоверные прогностические факторы риска развития гнойных осложнений со стороны послеоперационной раны у больных, перенесших плановые операции в многопрофильном стационаре. Несомненно, необходимы дальнейшие исследования с включением большего количества исследуемых факторов, групп оперативных вмешательств и числа больных. Однако уже на данном этапе полученные данные позволяют нам разрабатывать комплексные мероприятия, направленные на нивелирование влияния указанных факторов на исход плановых оперативных вмешательств в части снижения числа послеоперационных гнойных осложнений.
Благодарности
Работа выполнена без внешних источников финансирования.





Список литературы
Алешина Г.М. 2019. Лактоферрин – эндогенный регулятор защитных функций организма. Медицинский академический журнал, 19(1): 35–44.
Дибиров М.Д., Хачатрян Н.Н., Исаев А.И., Карсотьян Г.С., Алимова Э.Э., Костюк Е.А. 2019. Новые возможности антибактериальной терапии интраабдоминальных инфекций, вызванных полирезистентной микробной флорой. Хирургия, Том 2, 12: 74–83.
Зубрицкий В.Ф., Левчук А.Л., Фоминых Е.М. 2021. Хирургическая инфектология. М.: ДПК Пресс.
Киреева Е.М., Пашков А.Н., Пигачев А.В. 2021. Хирургическое лечение послеоперационного остеомиелита грудины. Огарёв-Online, 1(154): 1–5.
Князев В.Н., Фоминых Е.М., Мирошин С.И. 2022. Озоновая обработка поврежденных тканей на лечебно-эвакуационных этапах. Современные подходы к диагностике и лечению хирургических заболеваний, травм и их осложнений. Сборник трудов Общероссийской межведомственной науч.-практ. конф. М.: Редакция журнала «На боевом посту», 111–113.
Российские Национальные рекомендации по диагностике и лечению заболеваний артерий нижних конечностей. 2019.
СанПиН 3.3686-21 «Санитарно-эпидемиологические требования по профилактике инфекционных болезней», утверждены Главным государственным санитарным врачом РФ А.Ю. Поповой. 28.01.2021. https://www.rospotrebnadzor.ru/files/news/SP_infections_compressed.pdf
Шулакова Н.И., Тутельян А.В., Акимкин В.Г. 2021. Совершенствование информационного обеспечения эпидемиологического надзора за ИСМП. Сборник тезисов IX Конгресса с международным участием.
Arsalan-Werner A., Grisar P., Sauerbier M. 2020. Risk Factors for Reoperation in Primary Hand Infections: a Multivariate Analysis. Arch. Orthop. Trauma. Surg., 140(2): 283–288. doi: 10.1007/s00402-019-03306-4
Arulkumaran N., Routledge M., Schlebusch S. et al. 2020. Antimicrobial-Associated Harm in Critical Care: a Narrative Review. Intensive Care Med., 46: 225–235. doi: 10.1007/s00134-020-05929-3
Boussion K. et al. 2021. Epidemiology, Clinical Relevance and Prognosis of Staphylococci in Hospital-Acquired Postoperative Intra-Abdominal Infections: an Observational Study in Intensive Care Unit. Scientific Reports, 11: 5884.
Di Franco S., Alfieri A., Fiore M., Fittipaldi C., Pota V., Coppolino F., Sansone P., Pace M.C., Passavanti M.B. 2022. A Literature Overview of Secondary Peritonitis Due to Carbapenem-Resistant Ente-robacterales (CRE) in Intensive Care Unit (ICU) Patients. Antibiotics (Basel), 11(10): 1347. doi: 10.3390/ antibiotics11101347. PMID: 36290005; PMCID: PMC9598607
Gierek M., Ochała-Gierek G., Kitala D. 2022. Hidradenitis Suppurativa: Bacteriological Study in Surgical Treatment. Postepy Dermatol Alergol, 39(6): 1101–1105. doi: 10.5114/ada.2022. 119008. Epub 2022 Sep 9. PMID: 36686013; PMCID: PMC9837599.
Goswami K. 2020. Intraoperative and Postoperative Infection Prevention. J. Arthroplasty, 35(3S): S2-S8.
Guzin S., Ulrich V., Armin W. et al. 2021. Defining the Scope of Antimicrobial Stewardship Interventions on the Prescription Quality of Antibiotics for Surgical Intra-Abdominal Infections. Antibiotics, 10: 73.
Neupane S., Koirala D.P., Kharel S., Silwal S., Yadav K.K. 2022. Clinical Profile and Management of Perforation Peritonitis in Bharatpur Hospital, Nepal: A Prospective Study. Ann. Med. Surg. (Lond), 82: 104528. doi: 10.1016/ j.amsu.2022.104528. PMID: 36268443; PMCID: PMC9577425.
Oppelt P.U., Askevold I., Bender F. et al. 2021. Morgagni-Larrey Diaphragmatic Hernia Repair in Adult Patients: a Retrospective Single-Center. Hernia, 25(2): 479–489. doi: 10.1007/s10029-020-02147-0.
Pan J., Zhu Q., Zhang X., Xu J., Pan L., Mao X., Wu X. 2021. Factors Influencing the Prognosis of Patients with Intra-Abdominal Infection and Its Value in Assessing Prognosis. Infect. Drug. Resist., 14: 3425–3432. doi: 10.2147/ IDR.S325386. PMID: 34466008; PMCID: PMC8402985.
Payá-Llorente C., Martínez-López E., Sebastián-Tomás J.C., Santarrufina-Martínez S., de'Angelis N., Martínez-Pérez A. 2020. The Impact of Age and Comorbidity on the Postoperative Outcomes after Emergency Surgical Management of Complicated Intraabdominal Infections. Sci Rep., 10(1): 1631. doi: 10.1038/s 41598-020-58453-1. PMID: 32005885; PMCID: PMC6994579.
Pinto A.M., Cerqueira M.A., Bañobre-Lópes M. et al. 2020. Bacteriophages for Chronic Wound Treatment: from Traditional to Novel Delivery Systems. Viruses, 12(2): 235.
Pörner D., Von Vietinghoff S., Nattermann J., Strassburg C.P., Lutz P. 2021. Advances in the Pharmacological Management of Bacterial Peritonitis. Expert. Opin. Pharmacother, 22(12): 1567–1578.
Póvoa P., Moniz P., Pereira J.G., Coelho L. 2021. Optimizing Antimicrobial Drug Dosing in Critically Ill Patients. Microorga-nisms, 9(7): 1401. doi: 10.3390/ microorganisms 9071401. PMID: 34203510; PMCID: PMC8305961.
Nita M., Pliszczyński J., Kosieradzki M., Fiedor P. 2021. Review of the Latest Methods of Epidermolysis Bullosa and Other Chronic Wounds Treatment Including BIOOPA Dressing. Dermatol. Ther. doi: 10.1007/s13555-021-00578-w
Shukla R., Karagaiah P., Patil A. 2022. Surgical Treatment in Hidradenitis Suppurativa. J. Clin. Med., 11(9): 2311. doi: 10.3390/ jcm11092311. PMID: 35566438; PMCID: PMC9101712.