Методы визуализации в диагностике гипертрофической кардиомиопатии
Aннотация
Обзор посвящен методам визуализации сердца в диагностике, лечении и стратификации риска внезапной сердечной смерти у пациентов с гипертрофической кардиомиопатией (ГКМП). При работе с англо- и русскоязычными источниками использовались поисковые запросы по ключевым словам в базах данных e-Library, PubMed, Scopus и Web of Science за период с 2014 по 2023 гг. В обзоре представлены возможности эхокардиографического исследования в оценке наличия, распределения и выраженности гипертрофии миокарда, состояния митрального клапана и подклапанных структур, обструкции выносящего тракта левого желудочка, систолической и диастолической функций. Обсуждается роль компьютерной томографии, обладающей лучшими возможностями в более точной оценке толщины миокарда, анатомии коронарных артерий с идентификацией «миокардиального мостика». Подробно представлена магнитно-резонансная томография (МРТ) в диагностике и ведении больных ГКМП. Благодаря МРТ удаётся выявить различные фенотипы заболевания за счёт получения изображений высокого качества с резким контрастом между миокардом и кровотоком. Среди преимуществ метода МРТ отмечена возможность получения детализированных тканевых характеристик миокарда, что позволяет визуализировать очаги фиброза. Отмечено значение других методов визуализации, в частности однофотонной эмиссионной томографии, сцинтиграфии миокарда и коронароангиографии, в ведении больных ГКМП.
Ключевые слова: гипертрофическая кардиомиопатия, диагностика, методы визуализации, эхокардиография, компьютерная томография, магнитно-резонансная томография
Введение
В последние десятилетия отмечен существенный прорыв в изучении генетических особенностей и фенотипических проявлений гипертрофической кардиомиопатии (ГКМП). Благодаря достижениям в разработке и широкому применению методов визуализации получены дополнительные сведения об особенностях гипертрофии миокарда, прогнозировании риска внезапной сердечной смерти (ВСС) и эффективности лечения заболевания [Maron B., Maron M., 2016; Tower-Rader et al., 2020; Maron et al., 2022]. Диагноз ГКМП основывается на обнаружении с помощью методов визуализации необъяснимой и обычно асимметричной гипертрофии преимущественно левого желудочка (ЛЖ), что не может объясняться исключительно повышением нагрузки давлением при отсутствии другого сердечного или системного заболевания, метаболического или полиорганного синдрома, связанного с гипертрофией ЛЖ [Габрусенко и др., 2021; Elliott et al., 2014; Makavos et al., 2019].
Сначала эхокардиография (ЭхоКГ), затем магнитно-резонансная томография (МРТ), компьютерная томография (КТ) дополнили арсенал методов исследования и позволили улучшить диагностику ГКМП, детализировать особенности кардиальной патологии [Maron B., Maron M., 2016; Weissler-Snir et al., 2016; Wengrofsky et al., 2023].
Целью настоящего обзора является обсуждение возможностей современных методов визуализации в диагностике и ведении больных ГКМП.
Материалы и методы
При работе с источниками использовались поисковые запросы по ключевым словам в базах данных e-Library, PubMed, Scopus и Web of Science. В обзор были включены англо- и русскоязычные статьи, опубликованные за 10-летний период с 2014 по 2023 гг. В центре внимания фигурировали статьи, опубликованные в научных журналах, прошедших процедуру рецензирования.
Эхокардиография
ЭхоКГ является доступным и информативным методом в диагностике гипертрофии ЛЖ, что позволяет заподозрить её специфическую этиологию. Такая возможность объясняется способностью ЭхоКГ визуализировать гипертрофию, её выраженность и протяжённость, оценить размеры левого предсердия (ЛП), особенности митрального клапана (МК), подклапанных структур, наличие и выраженности обструкции, систолическую и диастолическую функции ЛЖ [Turvey et al., 2021]. Фенотипическое разнообразие и вариабельность клинических проявлений заболевания объясняют востребованность применения ЭхоКГ в получении дополнительной информации о гипертрофии и дифференциальной диагностике ГКМП с её фенокопиями, вторичной гипертрофией ЛЖ и другой кардиальной патологией [Lopes, Elliott, 2017; Robich et al., 2023].
Определение значительного утолщения стенки миокарда на любом уровне при недилатированном ЛЖ и отсутствии других причин, ответственных за такую степень гипертрофии, является характерным для ГКМП [Габрусенко и др., 2021; Elliott et al., 2014; Nagueh et al., 2022]. При ЭхоКГ может обнаруживаться увеличение толщины стенки желудочка любой локализации, включая стенки правого желудочка (ПЖ). При выполнении ЭхоКГ необходимо оценивать все доступные визуализации сегменты миокарда, отмечать наличие, протяженность и выраженность гипертрофии в соответствии со стандартным протоколом обследования из нескольких позиций. Для корректной оценки толщины миокарда, необходимо точное расположение и направление датчика вдоль ортогональных плоскостей, чтобы избежать косых сечений и переоценки размеров толщин стенок.
Диагноз ГКМП правомочен при определении максимальной толщины стенки как минимум одного сегмента миокарда ЛЖ ≥ 15 мм (или выше двух стандартных отклонений от нормы с поправкой на возраст, пол и рост) или ассиметричной гипертрофии межжелудочковой перегородки (МЖП). В пользу ГКМП свидетельствует соотношение толщины МЖП к задней стенке ЛЖ > 1,3 у нормотензивных и > 1,5 у пациентов с артериальной гипертензией [Haland, Edwardsen, 2020]. В случае выявления гипертрофии миокарда ЛЖ меньшей выраженности (13–14 мм), диагноз ГКМП ставится с учётом дополнительных признаков: семейный анамнез, изменения лабораторных показателей, на электрокардиограмме и результатов других методов визуализации [Elliott et al., 2014; Maron et al., 2022; Mitchell et al., 2023].
Точная оценка толщины стенки ЛЖ на всей её протяженности может быть осложнена, если гипертрофия ограничивается одним или двумя сегментами, особенно передней, переднебоковой стенки и верхушки ЛЖ. В таком случае используют ЭхоКГ-исследование с контрастированием или МРТ [Caiati et al., 2023] (рис. 1).
Примерно у 30–44 % встречается гипертрофия ПЖ, являющаяся предиктором неблагоприятного прогноза. Гипертрофия ПЖ считается при определении толщины стенки ˃ 5 мм, а при её значениях ˃ 10 мм гипертрофия расценивается как экстремальная [Keramida et al., 2020; Mandeş et al., 2020]. Обнаружение гипертрофии ПЖ при отсутствии вторичных причин может выступать дополнительным аргументом в пользу диагноза ГКМП. При измерении толщины свободной стенки ПЖ необходимо внимательно оценивать наличие слоя эпикардиального жира, который не следует включать в калькуляцию толщины.
Оценка митрального клапана
Существовавшее ранее мнение, что поражение сердца при ГКМП ограничено лишь миокардом желудочков, претерпело изменения. Примерно у 60 % пациентов с диагнозом ГКМП выявляют, по крайней мере, одну аномалию МК как прямое следствие генетических мутаций [Mandeş et al., 2020; Sherrid, Adams, 2020]. К частым признакам относят удлинение створок и хорд МК, пролапс створок, прямое прикрепление сосочковой мышцы к передней створке МК, гипертрофию и диспозицию сосочковых мышц [Cardim et al., 2015; Sakellaropoulos et al., 2021; Malcolmson et al., 2023].
Переднее систолическое движение (SAM) МК, описанное впервые в конце 1960-х, сейчас считается специфичным проявлением ГКМП с частотой встречаемости до 31–61 % и основным патофизиологическим событием, ответственным за обструкцию выносящего тракта ЛЖ (ВТЛЖ) [Guigui et al., 2022]. О тяжести SAM можно судить в М-режиме по продолжительности контакта створки/хорды МК с МЖП, который считается умеренным, если длительность контакта не превышает 10 % систолы, и выраженным, если ˃ 30 % [Williams et al., 2009].
Митральная недостаточность, выявляемая у пациентов с ГКМП, может быть следствием аномалии МК, SAM или сопутствующей патологии МК.
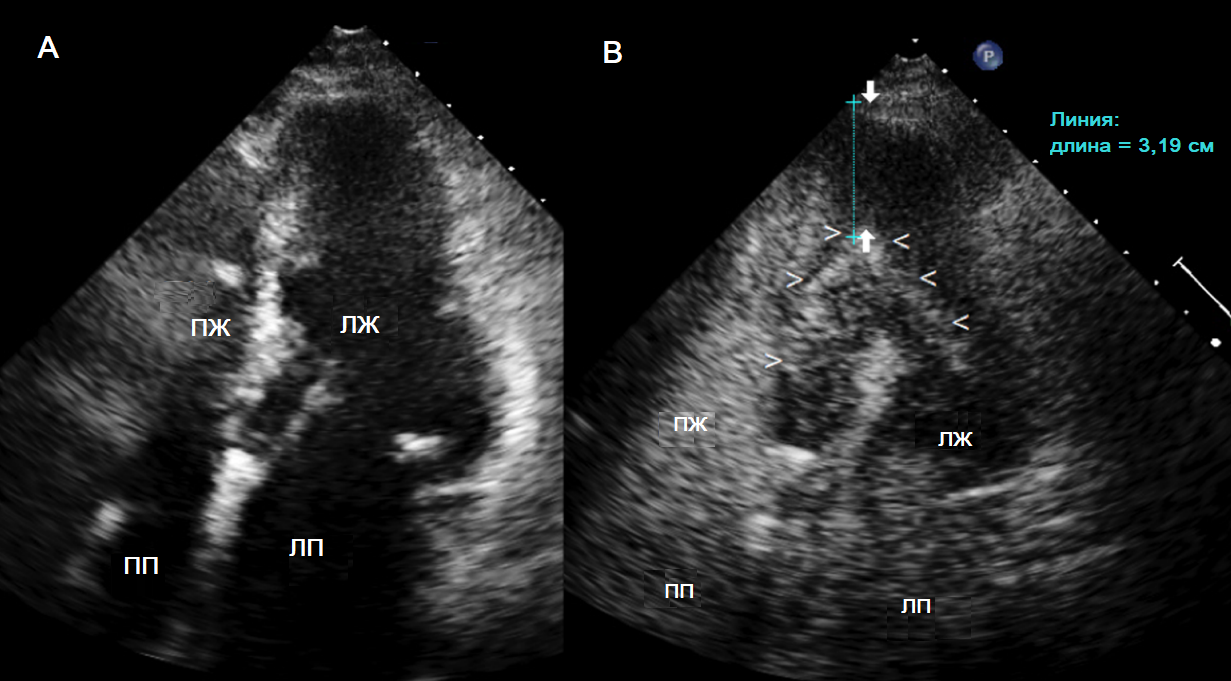 Рис. 1. Апикальный вариант гипертрофической кардиомиопатии. А. В области верхушки левого желудочка (ЛЖ) отмечается плохое разграничение эндокарда и полости сердца. В. После введения контрастного вещества четко видны очертания эндокарда верхушки (отмечено стрелками). Выраженная гипертрофия апикальной стенки ЛЖ (толщина 3,19 см). ПЖ – правый желудочек; ПП – правое предсердие; ЛП – левое предсердие. Адаптировано из Caiati et al. [Caiati, 2023]
Рис. 1. Апикальный вариант гипертрофической кардиомиопатии. А. В области верхушки левого желудочка (ЛЖ) отмечается плохое разграничение эндокарда и полости сердца. В. После введения контрастного вещества четко видны очертания эндокарда верхушки (отмечено стрелками). Выраженная гипертрофия апикальной стенки ЛЖ (толщина 3,19 см). ПЖ – правый желудочек; ПП – правое предсердие; ЛП – левое предсердие. Адаптировано из Caiati et al. [Caiati, 2023]
Fig. 1. Apical variant of hypertrophic cardiomyopathy. A. The left ventricular (LV) apical region does not show any clear delineation of the endocardial border. B. After contrast injection, a perfect delineation of the true apical endocardium is very clearly depicted as a hyper reflective line of backscatter (arrowheads). The severe hypertrophy of the LV apical wall (3,19 cm thickness). RV = right ventricle; RA = right atrium; LA = left atrium. Adapted from Caiati et al. [Caiati, 2023]
Обструкция выносящего тракта левого желудочка
С клинической точки зрения чрезвычайно важно различать варианты ГКМП с и без обструкции ВТЛЖ, что влияет на оценку прогноза заболевания и выбор лечебной стратегии. Выраженная обструкция ВТЛЖ (˃30 мм рт. ст.) ассоциируется с худшим прогнозом и является предиктором сердечной недостаточности и смертности больных. Обструкция ВТЛЖ устанавливается при наличии градиента давления ВТЛЖ > 30 мм рт. ст. в покое или во время физиологической провокации (проба Вальсавы, вставание, выполнение упражнений). У больных ГКМП отмечается широкий разброс значений градиента, который иногда достигает 200 мм рт. ст. и более [Игнатенко и др., 2022; Geske et al, 2022]. Градиент более 50 мм рт. ст. считается гемодинамически значимым и требует обсуждения применения хирургических методов лечения кардиомиопатии.
Генез обструкции ВТЛЖ многофакторный и обусловлен выраженной гипертрофией базального отдела МЖП, анатомическими особенностями МК и подклапанного аппарата, феноменом SAM и меньшим аортосептальным углом [Jain et al., 2019; Fumagalli et al., 2022; Monda et al., 2022]. Примерно треть пациентов ГКМП не имеют обструкции ВТЛЖ, в то время как другие демонстрируют динамическую обструкцию при минимальной гипертрофии МЖП. Среднежелудочковая обструкция обычно наблюдается у пациентов со значительной гипертрофией ЛЖ в средней части МЖП и уменьшением его полости (ЛЖ по типу «песочных часов») [Nie et al., 2022].
Оценка наличия и выраженности обструкции производится с применением двухмерной ЭхоКГ и допплеровского режима по значениям скорости среднего и максимального кровотока на уровне ВТЛЖ. Как правило, при ГКМП скорость кровотока медленно увеличивается в начале систолы, затем резко возрастает и достигает пика в середине-конце систолы, что приводит к характерной «кинжалообразной» кривой. Максимальный мгновенный градиент, отражающий выраженность обструкции, определяется путем измерения пиковой скорости на уровне ВТЛЖ с использованием непрерывного допплеровского метода и вычисляется по упрощенному уравнению Бернулли (градиент ВТЛЖ = 4 x V2, где V – скорость кровотока в м/с) [Nagueh et al., 2022].
Обструкция при ГКМП является довольно динамической, и её выраженность зависит от параметров пред-, постнагрузки и сократительной способности миокарда. У пациентов без обструкции в покое рекомендуется измерение скорости градиента в ВТЛЖ во время пробы Вальсальвы в сидячем положении и полулёжа на спине с последующим вставанием, провоцирующей его появление (или прирост) [Zemanek et al., 2015; Rowin et al., 2017]. Если маневры с положением тела не позволяют индуцировать появление градиента обструкции ВТЛЖ ≥ 50 мм рт. ст., рекомендуется выполнять стресс-ЭхоКГ с физической нагрузкой [Stewart et al., 2023]. Физические упражнения в контролируемых условиях являются предпочтительной нагрузкой для стимуляции градиента в силу наиболее реалистичного воспроизведения физической активности, которая характерна для пациентов в повседневной жизни. В связи с этим, а также из-за нередко плохой переносимости, фармакологическая провокация добутамином не рекомендуется у больных ГКМП [Elliott et al., 2014; Rowin et al., 2017].
Систолическая функция левого желудочка
ЭхоКГ является информативным методом изучения систолической функции ЛЖ по оценке параметров глобальной сократимости, в частности фракции выброса (ФВ) ЛЖ. У большинства больных ГКМП значения ФВЛЖ находятся в пределах нормы или даже выше, свидетельствуя о гиперконтрактильном состоянии миокарда. Дисфункция ЛЖ, определяемая по ФВ < 50 %, наблюдается у 4–9 % больных и ассоциируется с высокими уровнями общей смертности, трансплантацией сердца и имплантацией устройств вспомогательного кровообращения [Marstrand et al., 2020]. Оценка систолической функции ЛЖ может быть сложной задачей у пациентов с большими апикальными аневризмами.
При ГКМП анализ систолической деформации и скорости деформации демонстрируют ряд региональных и глобальных нарушений, даже у пациентов с нормальными показателями ФВ. Нарушения систолической деформации и скорости деформации связаны, по-видимому, в основном с региональной гипертрофией и выявляются в МЖП при «классической» септальной гипертрофии и на верхушке – при апикальном варианте [Urbano-Moral et al., 2014; Nagueh et al., 2022]. Следует отметить, что у пациентов с ГКМП со значительной гипертрофией, несмотря на сохранную ФВ, часто регистрируются низкие значения конечно-диастолического и ударного объема ЛЖ.
Диастолическая функция левого желудочка
Одним из основных патофизиологических механизмов сердечной недостаточности у пациентов с ГКМП является диастолическая дисфункция, обусловленная увеличением массы и жесткости ЛЖ, что отмечается уже на ранних стадиях заболевания. Изменения релаксации и наполнения ЛЖ и ЛП отмечаются практически у 90 % больных ГКМП. Полагают, что диастолическая дисфункция обусловлена ишемией миокарда, миокардиальным фиброзом, нарушением функции ЛП и предсердной миопатией. Состояние диастолической функции влияет на прогноз заболевания: пациенты с нарушением диастолического наполнения ЛЖ подвержены более высокому риску неблагоприятного исхода даже при сохранной ФВ [Nagueh et al., 2016].
Допплер-ЭхоКГ представляет собой чувствительный метод оценки диастолической функции, но на её результаты оказывают влияние такие факторы, как частота сердечных сокращений, возраст больных и условия нагрузки. Важно отметить, что у больных ГКМП полученные параметры трансмитрального кровотока (пик Е, Е/А-соотношение и время замедления) плохо коррелируют с конечно-диастолическим давлением ЛЖ [Williams et al., 2009]. Показано, что соотношение E∕e с использованием тканевого допплеровского картирования (TDI) предоставляет более точную оценку конечно-диастолического давления ЛЖ при этой патологии. При исследовании диастолической функции рекомендуется комплексный подход с изучением показателей трансмитрального кровотока, TDI митрального кольца, скоростей кровотока в легочных венах, объёма и размера ЛП, максимальной скорости трикуспидальной регургитации [Elliott et al., 2014].
Трансэзофагеальная эхокардиография
Трансэзофагеальная ЭхоКГ (ТЭЭ) оправдана у пациентов при неинформативных данных трансторакальной ЭхоКГ в качестве альтернативы или дополнения к МРТ. ТЭЭ, в частности, показана пациентам с обструкцией ВТЛЖ, если её механизм остаётся не ясен, при оценке МК или когда предполагается значительная митральная регургитация вследствие поражения самого клапана [Габрусенко и др., 2021]. Во время выполнения хирургической миэктомии ТЭЭ выполняется для визуального контроля процедуры и возможных осложнений (дефект МЖП, аортальная регургитация и резидуальная обструкция ВТЛЖ) [Elliott et al., 2014].
Таким образом, ЭхоКГ является информативным методом у пациентов с ГКМП, позволяющим первоначально установить диагноз, оценить особенности гипертрофии миокарда желудочков. ЭхоКГ позволяет выявить обструкцию в ВТЛЖ и на среднежелудочковом уровне, оценить градиент, а также получить важную информацию об особенностях строения и функции МК, подклапанного аппарата. На основании анализа литературных данных и собственного опыта мы полагаем чрезвычайно важным больным с подозрением на ГКМП проводить полноценное ЭхоКГ-исследование с измерением толщин миокарда всех доступных для лоцирования стенок правого и ЛЖ. Кроме того, ЭхоКГ предоставляет надёжные данные в отношении размеров и функции ЛП и ЛЖ. ЭхоКГ, выполняемая в течение периода наблюдения за пациентами, помогает разрабатывать и проводить оптимальную лечебную программу, мониторировать динамику основных показателей, прогнозировать течение и исход заболевания.
Компьютерная томография сердца
КТ предоставляет прекрасное пространственное разрешение с чёткой визуализацией структур ЛЖ, что позволяет выявить гипертрофию миокарда, оценить папиллярные мышцы, а также точно измерить толщины стенок желудочков (рис. 2) [Oliveira et al., 2016; Ommen et al., 2020; Panetta et al., 2021].
Кроме оценки геометрии и функции камер сердца, КТ используется для определения анатомии клапанного аппарата сердца и коронарных артерий (КА), в том числе стеноза и аномалий отхождения [Oliveira et al., 2016]. Боль в грудной клетке – довольно распространенный клинический симптом при ГКМП, в происхождении которого выделяют несколько механизмов, включая увеличение постнагрузки и ишемию миокарда [Weissler-Snir et al., 2016]. Одной из причин ишемии миокарда является наличие «миокардиального мостика» (myocardial bridging), который представляет врожденную аномалию, при которой сегмент эпикардиальной КА (обычно левой передней нисходящей) проходит под миокардиальным слоем и, по данным аутопсий, регистрируется примерно у 40 % больных [Габрусенко и др., 2021; Weissler-Snir et al., 2016].
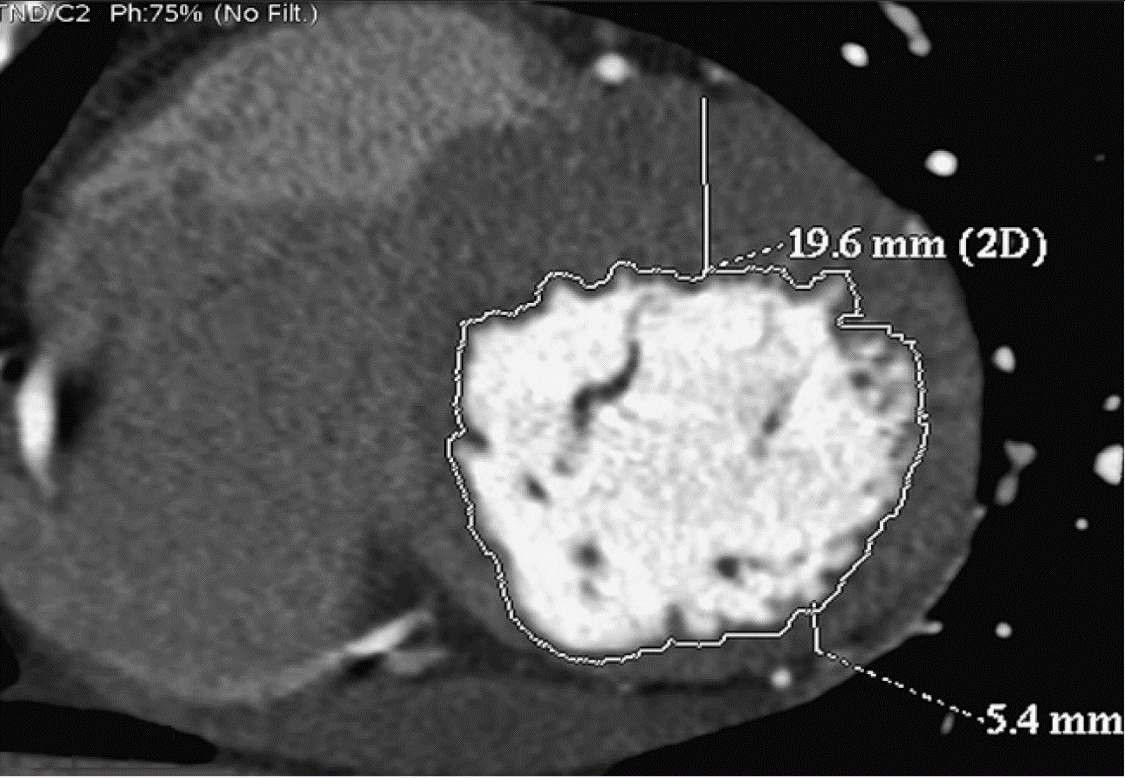 Рис. 2. Снимок компьютерной томографии сердца по короткой оси, на котором представлена асимметричная гипертрофия миокарда. Толщина передней части межжелудочковой перегородки – 19,6 мм и нижнебоковой стенки левого желудочка – 5,4 мм. Адаптировано из Nagueh et al. [Nagueh et al., 2011]
Рис. 2. Снимок компьютерной томографии сердца по короткой оси, на котором представлена асимметричная гипертрофия миокарда. Толщина передней части межжелудочковой перегородки – 19,6 мм и нижнебоковой стенки левого желудочка – 5,4 мм. Адаптировано из Nagueh et al. [Nagueh et al., 2011]
Fig. 2. Short-axis cardiac computed tomographic image demonstrating asymmetric myocardial hypertrophy. The measurements shown are those of the anterior septum (19.6 mm) and inferolateral wall (5.4 mm). Adapted from Nagueh et al. [Nagueh et al., 2011]
Европейское руководство по ведению больных с ГКМП рекомендует выполнять КТ у пациентов с плохим акустическим окном для ЭхоКГ и противопоказаниями к МРТ [Elliott et al., 2014]. Несмотря на широкий диапазон клинических возможностей, КТ показана лишь в сложных для постановки диагноза случаях или при невозможности выполнить другие методы исследования. КТ сердца является информативным методом исключения обструктивного атеросклеротического поражения КА и «мышечного мостика». К недостаткам КТ по сравнению с МРТ можно отнести более низкое временное разрешение и наличие ионизирующего излучения.
Магнитно-резонансная томография сердца
Выполнение МРТ позволяет получить детальную информацию относительно морфологии, функции желудочков, характеристики миокарда у больных с установленным или предполагаемым диагнозом «ГКМП» [Малов и др., 2020]. В 2015 г. экспертами Европейской ассоциации сердечно-сосудистой визуализации [Cardim et al., 2015] отмечено, что МРТ сердца следует рассматривать при изначальном обследовании всех пациентов с ГКМП, если позволяют технические ресурсы и опыт персонала. МРТ обеспечивает полный захват обоих желудочков и является «золотым стандартом» для оценки толщины стенок и объемов камер с высоким пространственным и временным разрешением в любом месте без ионизирующего излучения. Более того, МРТ интегрирована в мультимодальный подход визуализации, включая ЭхоКГ и КТ [Cardim et al., 2015; Casas, Rodríguez-Palomares, 2022; Rashdan et al., 2023; Wengrofsky et al., 2023].
В последних рекомендациях 2020 г. Американской Ассоциации Сердца и Американской Коллегии Кардиологов [Ommen et al., 2020] по диагностике и лечению ГКМП отмечена возрастающая роль МРТ в улучшении качества диагностики, стратификации риска ВСС и семейного скрининга заболевания. МРТ идеально подходит для изучения множества фенотипов ГКМП, обеспечивая изображения высокого качества, с резким контрастом между границами миокарда и кровотоком, а также томографическую реконструкцию сердца с визуализацией всех сегментов ЛЖ [Hindieh et al., 2017; Casas, Rodríguez-Palomares, 2022].
МРТ незаменима при постановке диагноза «ГКМП» у пациентов с плохим акустическим окном или когда некоторые участки ЛЖ и ПЖ визуализируются недостаточно качественно [Hindieh et al., 2017; Quarta et al., 2018]. При измерении массы миокарда ЛЖ данные МРТ более предпочтительны, чем трансторакальной ЭхоКГ [Dong et al., 2023; Rashdan et al., 2023]. Получаемые изображения не зависят от конституции тела, формы грудной клетки, паренхиматозного заболевания легких, которые ограничивают ультразвуковое окно [Geske et al., 2018]. МРТ обладает бесспорными преимуществами в идентификации верхушечной, переднебоковой гипертрофии, аневризм, интракардиальных тромбов и трудно визуализируемых патологических изменений при ГКМП, таких как миокардиальные крипты и аномалии папиллярных мышц [Малов и др., 2020; Maron et al., 2014; Hughes, 2023].
Вероятно, наибольшей ценностью МРТ сердца при ведении больных ГКМП является предоставление тканевых характеристик миокарда. Применение таких возможностей, как обнуление миокарда и оценка T2-взвешенного изображения, помогает исключить фенокопии, в частности амилоидоз сердца и гемохроматоз. Использование позднего усиления гадолиния (LGE) обеспечивает определение участков фиброза миокарда in vivo, что обнаруживается у 80 % больных ГКМП [Hoey et al., 2014; Geske et al., 2018; Monda et al., 2022] (рис. 3). Обширные участки LGE свидетельствуют о неблагоприятном прогнозе, при этом многочисленные исследования демонстрируют корреляцию LGE с увеличенной толщиной стенки миокарда, проявлениями ишемии, сниженной ФВ, неустойчивой желудочковой тахикардией и смертностью [Мершина и др., 2019; Chan et al., 2014; Tower-Rader et al., 2020; Lander et al., 2022]. При показателях количественной оценки LGE в размере 15 % от площади миокарда отмечено увеличение числа случаев ВСС в 2 раза [Chan et al., 2014; MacNamara, Link, 2023].
В отличие от трансторакальной ЭхоКГ, которая даёт возможность изначально поставить диагноз «ГКМП», МРТ благодаря лучшей пространственной визуализации и более точным результатам измерения толщин стенок сердца позволяет выявить различные фенотипы локальной гипертрофии миокарда и определить фенотипический вариант заболевания. Кроме того, бесспорным преимуществом МРТ является получение тканевых характеристик миокарда, что позволяет идентифицировать больных, имеющих высокий риск ВСС.
Другие методы визуализации
Другие методы диагностики, включая однофотонную эмиссионную КТ, позитронную эмиссионную томографию (PET), сцинтиграфию миокарда и коронароангиографию (КАГ), применяют при ГКМП, как правило, для дифференциальной диагностики, определения поражений коронарного и микроциркуляторного русла [Габрусенко и др., 2021; Bravo, 2019; Nagueh et al., 2022].
Однофотонная эмиссионная КТ с использованием радиоактивного хлорида таллия помогает выявить нарушения перфузии миокарда. Визуализация аномальной перфузии у больных ГКМП при нагрузочных состояниях ассоциируется с повышенным риском обмороков, снижением толерантности к физической нагрузке, высокими уровнями сердечно-сосудистой смертности и ВСС [Weissler-Snir et al., 2016].
Имеющиеся на сегодняшний день данные подтверждают клиническую значимость количественной визуальной оценки с помощью PET у больных ГКМП в выявлении ишемии миокарда, оценке тяжести микрососудистой дисфункции и в качестве перспективного предиктора в прогнозировании неблагоприятных сердечно-сосудистых исходов. Учитывая отсутствие обоснованных рекомендаций в пользу или против PET для стратификации риска желудочковых тахиаритмий и ВСС, необходимы дальнейшие исследования, посвященные изучению роли количественной оценки миокардиального кровотока в стратификации риска, особенно в сочетании с оценкой фиброза миокарда [Bravo, 2019].

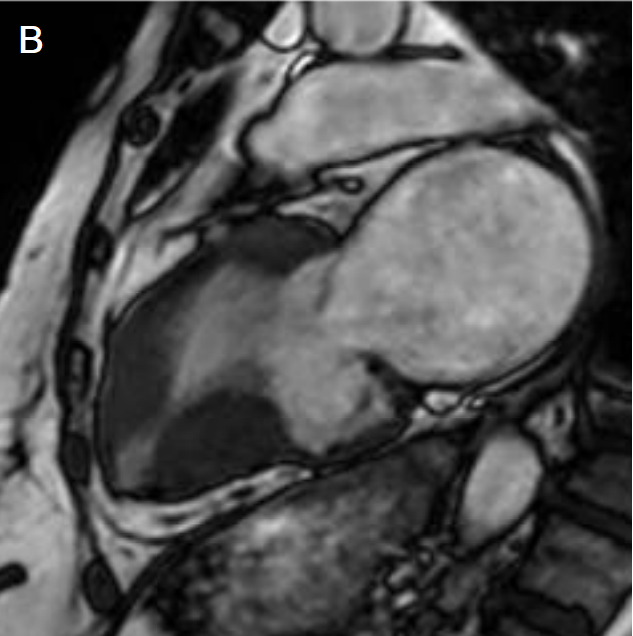
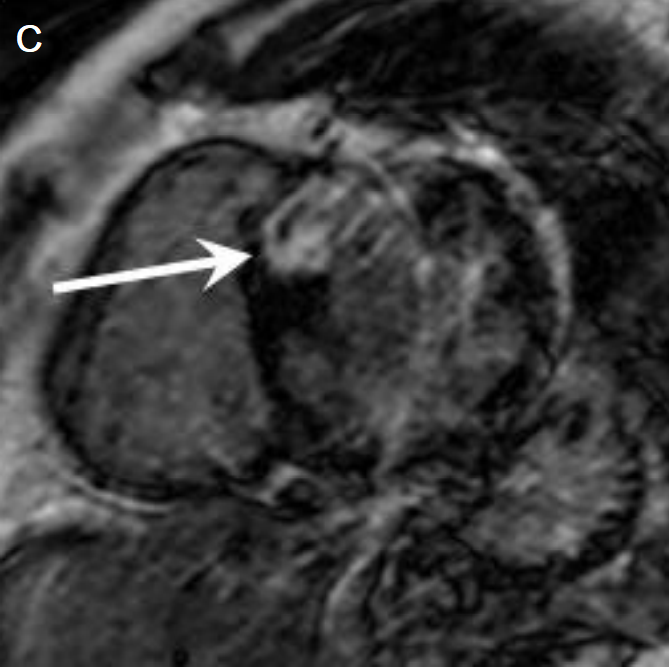
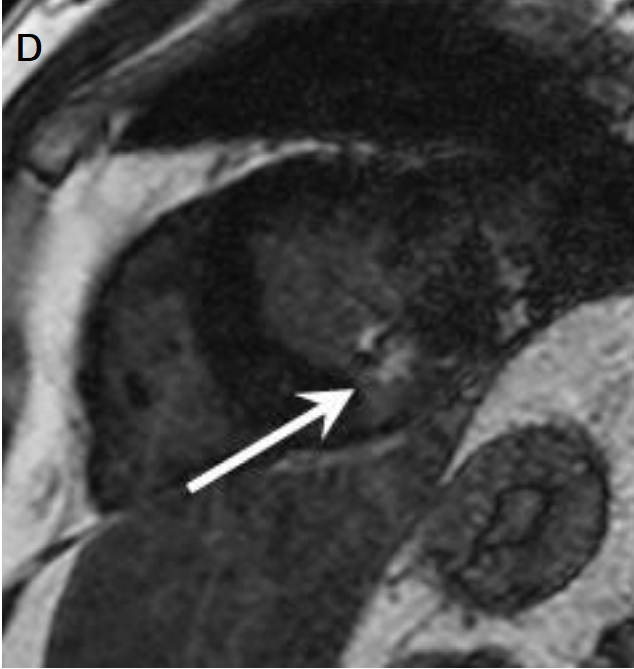
Рис. 3. Изображения магнитно-резонансной томографии сердца при двух фенотипах гипертрофической кардиомиопатии. Панели А и B: кадры четырехкамерной позиции в режиме свободной прецессии в установившемся состоянии (диастола). На рис. В отмечается значительное увеличение левого предсердия, сравнимое по размерам с левым желудочком (ЛЖ); С и D – позднее усиление гадолиния, свидетельствующее об очагах фиброза (отмечены стрелками). МЖП – межжелудочковая перегородка. Адаптировано из Hoey et al. [Hoey et al., 2014].
Fig. 3. Two HCM phenotypes assessed with MRI. A and B: diastolic SSFP the images (diastole) from four-chamber view images with corresponding late gadolinium enhancement images (С, D). B: significant left atrial enlargement comparable to the left ventricle by dimensions. In С and D images there is patchy mid-wall fibrosis demonstrated on the late gadolinium enhanced images (arrows). HCM, hypertrophic cardiomyopathy; MRI, magnetic resonance imaging; SSFP, steady state free precession. Adapted from Hoey et al. [Hoey et al., 2014].
Выполнение КАГ при ГКМП рекомендуется больным с имеющимися симптомами или проявлениями ишемии миокарда, с предотвращенными случаями внезапной остановки сердца, устойчивой желудочковой тахикардией для исключения обструктивного поражения КА [Габрусенко и др., 2021]. Кроме того, КАГ показана больным, имеющим факторы риска коронарного атеросклероза до выполнения хирургической миэктомии.
Заключение
В настоящее время методы визуализации играют ведущую роль в диагностике ГКМП, определении фенотипов, обструкции среднежелудочкового отдела и на уровне ВТЛЖ, стратификации риска ВСС и мониторировании течения заболевания. ЭхоКГ благодаря своей доступности и информативности выступает в качестве первичного метода, используемого в постановке диагноза. Ведение больных ГКМП требует применения мультимодального режима визуализации при наличии возможностей и соответствующего опыта персонала, что позволяет получить более полную информацию о локализации и распространенности гипертрофии, особенностях клапанного аппарата, КА, тканевых характеристик миокарда.
Благодарности
Работа выполнена без внешних источников финансирования.





Список литературы
Габрусенко С.А., Гудкова А.Я., Козиолова Н.А., Александрова С.А., Берсенева М.И., Гордеев М.Л., Дземешкевич С.Л., Заклязьминская Е.В., Иртюга О.Б., Каплунова В.Ю., Костарева А.А., Крутиков А.Н., Маленков Д.А., Новикова Т.Н., Саидова М.А., Санакоев М.К., Стукалова О.В. 2021. Гипертрофическая кардиомиопатия. Клинические рекомендации 2020. Российский кардиологический журнал, 26(5): 269–334. doi:10.15829/1560-4071-2021-4541
Игнатенко Г.А., Тарадин Г.Г., Ракитская И.В., Ковальчук Н.О., Могилевская К.Э. 2022. Выраженная обструкция выносящего тракта левого желудочка при гипертрофической кардиомиопатии. Вестник неотложной и восстановительной хирургии. 7(1): 112–124.
Малов А.А., Джорджикия Р.К., Абушаев А.И. 2020. Диагностические возможности магнитно-резонансной томографии сердца в дифференциальной диагностике фенотипических форм гипертрофической кардиомиопатии. Лучевая диагностика и терапия, 11(4): 44–51. doi:10.22328/2079-5343-2020-11-4-44-51
Мершина Е.А., Синицын В.Е., Ларина О.М. 2019. Магнитно-резонансная томография сердца в диагностике гипертрофической кардиомиопатии и стратификации риска внезапной сердечной смерти. Клиническая и экспериментальная хирургия, 7(3), 70–78. doi: 10.24411/2308-1198-2019-13008
Bravo P.E. 2019. Is there a role for cardiac positron emission tomography in hypertrophic cardiomyopathy? Journal of nuclear cardiology: official publication of the American Society of Nuclear Cardiology, 26(4), 1125–1134. doi: 10.1007/s12350-018-1298-4
Caiati C., Stanca A., Lepera M.E. 2023. Case report: Diagnosis of apical hypertrophic cardiomyopathy that escaped clinical and echocardiographic investigations for twenty years: Reasons and clinical implications. Frontiers in cardiovascular medicine, 10, 1157599. doi:10.3389/fcvm.2023.1157599
Cardim N., Galderisi M., Edvardsen T., Plein S., Popescu B.A., D'Andrea A., Bruder O., Cosyns B., Davin L., Donal E., Freitas A., Habib G., Kitsiou A., Petersen S.E., Schroeder S., Lancellotti P., Camici P., Dulgheru R., Hagendorff A., Lombardi M., … Sicari R. 2015. Role of multimodality cardiac imaging in the management of patients with hypertrophic cardiomyopathy: an expert consensus of the European Association of Cardiovascular Imaging Endorsed by the Saudi Heart Association. European heart journal. Cardiovascular Imaging, 16(3), 280.doi: 10.1093/ehjci/jeu291
Casas G., Rodríguez-Palomares J.F. 2022. Multimodality cardiac imaging in cardiomyopathies: from diagnosis to prognosis. Journal of clinical medicine, 11(3), 578. doi: 10.3390/jcm11030578
Chan R.H, Maron B.J., Olivotto I., Pencina M.J., Assenza G.E., Haas T., Lesser J.R., Gruner C., Crean A.M., Rakowski H., Udelson J.E., Rowin E., Lombardi M., Cecchi F., Tomberli B., Spirito P., Formisano F., Biagini E., Rapezzi C., De Cecco C.N., … Maron M.S. 2014. Prognostic value of quantitative contrast-enhanced cardiovascular magnetic resonance for the evaluation of sudden death risk in patients with hypertrophic cardiomyopathy. Circulation, 130(6), 484–495. doi: 10.1161/CIRCULATIONAHA.113.007094
Dong T., Gilliland Y., Kramer C.M., Theodore A., Desai M. 2023. Multimodality imaging of hypertrophic cardiomyopathy. Progress in cardiovascular diseases, S0033-0620(23)00079-8. Advance online publication. doi: 10.1016/j.pcad.2023.08.004
Fumagalli I., Vitullo P., Vergara C., Fedele M., Corno A.F., Ippolito S., Scrofani R., Quarteroni A. 2022. Image-based computational hemodynamics analysis of systolic obstruction in hypertrophic cardiomyopathy. Frontiers in physiology, 12, 787082. doi: 10.3389/fphys.2021.787082
Geske J.B., Ommen S.R., Gersh B.J. 2018. Hypertrophic cardiomyopathy: clinical update. JACC. Heart failure, 6(5), 364–375. doi: 10.1016/j.jchf.2018.02.010
Geske J.B., Stephens E.H., Dearani J.A. 2022. Hypertrophic cardiomyopathy with extreme outflow tract obstruction. European heart journal, 43(42), 4518. doi: 10.1093/eurheartj/ehac439
Guigui S.A., Torres C., Escolar E., Mihos C.G. 2022. Systolic anterior motion of the mitral valve in hypertrophic cardiomyopathy: a narrative review. Journal of thoracic disease, 14(6), 2309–2325. doi: 10.21037/jtd-22-182
Elliott P.M., Anastasakis A., Borger M.A., Borggrefe M., Cecchi F., Charron P., Hagege A.A., Lafont A., Limongelli G., Mahrholdt H., McKenna W.J., Mogensen J., Nihoyannopoulos P., Nistri S., Pieper P.G., Pieske B., Rapezzi C., Rutten F.H., Tillmanns C., … Watkins H. 2014. 2014 ESC Guidelines on diagnosis and management of hypertrophic cardiomyopathy: the Task Force for the Diagnosis and Management of Hypertrophic Cardiomyopathy of the European Society of Cardiology (ESC). European heart journal, 35(39), 2733–2779. doi: 10.1093/eurheartj/ehu284
Haland T.F., Edvardsen T. 2020. The role of echocardiography in management of hypertrophic cardiomyopathy. Journal of echocardiography, 18(2), 77–85. doi: 10.1007/s12574-019-00454-9
Hindieh W., Chan R., Rakowski H. 2017. Complementary role of echocardiography and cardiac magnetic resonance in hypertrophic cardiomyopathy. Current cardiology reports, 19(9), 81. doi: 10.1007/s11886-017-0897-z
Hoey E.T., Elassaly M., Ganeshan A., Watkin R.W., Simpson H. 2014. The role of magnetic resonance imaging in hypertrophic cardiomyopathy. Quantitative imaging in medicine and surgery, 4(5), 397–406. doi: 10.3978/j.issn.2223-4292.2014.09.04
Hughes R.K., Knott K.D., Malcolmson J., Augusto J.B., Kellman P., Moon J.C., Captur G. 2020. Advanced imaging insights in apical hypertrophic cardiomyopathy. JACC. Cardiovascular imaging, 13(2 Pt 2), 624–630. doi: 10.1016/j.jcmg.2019.09.010
Jain C.C., Newman D.B., Geske J.B. 2019. Mitral valve disease in hypertrophic cardiomyopathy: evaluation and management. Current cardiology reports, 21(11), 136. doi: 10.1007/s11886-019-1231-8
Keramida K., Lazaros G., Nihoyannopoulos P. 2020. Right ventricular involvement in hypertrophic cardiomyopathy: Patterns and implications. Hellenic journal of cardiology: HJC = Hellenike kardiologike epitheorese, 61(1), 3–8. doi: 10.1016/j.hjc.2018.11.009
Lander B.S., Zhao Y., Hasegawa K., Maurer M.S., Tower-Rader A., Fifer M.A., Reilly M.P., Shimada Y.J. 2022. Comprehensive proteomics profiling identifies patients with late gadolinium enhancement on cardiac magnetic resonance imaging in the hypertrophic cardiomyopathy population. Frontiers in cardiovascular medicine, 9, 839409. doi: 10.3389/fcvm.2022.839409
Lopes L.R., Elliott P.M. Hypertrophic cardiomyopathies. In: Hurst’s the Heart. Ed. by V. Fuster et al, McGraw-Hill Education, 2017. − 14th ed. Chapter 59. P. 1443–1464.
MacNamara J.P., Link M.S. 2023. Cardiac magnetic resonance imaging continues as a cornerstone of the assessment of hypertrophic cardiomyopathy. Heart rhythm, 20(7), 968–969. doi: 10.1016/j.hrthm.2023.04.002
Makavos G., Κairis C., Tselegkidi M.E., Karamitsos T., Rigopoulos A.G., Noutsias M., Ikonomidis I. 2019. Hypertrophic cardiomyopathy: an updated review on diagnosis, prognosis, and treatment. Heart failure reviews, 24(4), 439–459. doi: 10.1007/s10741-019-09775-4
Malcolmson J., Shipolini A., Mohiddin S., Savvatis K. 2023. The mitral valve in hypertrophic cardiomyopathy. Current opinion in cardiology, 38(5), 415–423. doi: 10.1097/HCO.0000000000001067
Mandeş L., Roşca M., Ciupercă D., Popescu B.A. 2020. The role of echocardiography for diagnosis and prognostic stratification in hypertrophic cardiomyopathy. Journal of echocardiography, 18(3), 137–148. doi: 10.1007/s12574-020-00467-9
Maron B.J., Ommen S.R., Semsarian C., Spirito P., Olivotto I., Maron M.S. 2014. Hypertrophic cardiomyopathy: present and future, with translation into contemporary cardiovascular medicine. Journal of the American College of Cardiology, 64(1), 83–99. doi: 10.1016/j.jacc.2014.05.003
Maron B.J., Maron M.S. 2016. The Remarkable 50 years of imaging in HCM and how it has changed diagnosis and management: from M-mode echocardiography to CMR. JACC. Cardiovascular imaging, 9(7), 858–872. doi: 10.1016/j.jcmg.2016.05.003
Maron B.J., Desai M.Y., Nishimura R.A., Spirito P., Rakowski H., Towbin J.A., Rowin E.J., Maron M.S., Sherrid M.V. 2022. Diagnosis and evaluation of hypertrophic cardiomyopathy: JACC State-of-the-Art Review. Journal of the American College of Cardiology, 79(4), 372–389. doi: 10.1016/j.jacc.2021.12.002
Marstrand P., Han L., Day S.M., Olivotto I., Ashley E.A., Michels M., Pereira A.C., Wittekind S.G., Helms A., Saberi S., Jacoby D., Ware J.S., Colan S.D., Semsarian C., Ingles J., Lakdawala N.K., Ho C.Y., SHaRe Investigators 2020. Hypertrophic cardiomyopathy with left ventricular systolic dysfunction: insights from the SHaRe Registry. Circulation, 141(17), 1371–1383. doi: 10.1161/CIRCULATIONAHA.119.044366
Mitchell C.C., Frye C., Jankowski M., Symanski J., Lester S.J., Woo A., Gilliland Y., Dragulescu A., Abraham T., Desai M., Martinez M.W., Nagueh S.F., Phelan D. 2023. A practical approach to echocardiographic imaging in patients with hypertrophic cardiomyopathy. Journal of the American Society of Echocardiography: official publication of the American Society of Echocardiography, S0894-7317(23)00249-3. doi: 10.1016/j.echo.2023.04.020
Monda E., Palmiero G., Lioncino M., Rubino M., Cirillo A., Fusco A., Caiazza M., Verrillo F., Diana G., Mauriello A., Iavarone M., Losi M.A., De Rimini M.L., Dellegrottaglie S., D'Andrea A., Bossone E., Pacileo G., Limongelli G. 2022. Multimodality imaging in cardiomyopathies with hypertrophic phenotypes. Journal of clinical medicine, 11(3), 868. doi: 10.3390/jcm11030868
Nagueh S.F., Bierig S.M., Budoff M.J., Desai M., Dilsizian V., Eidem B., Goldstein S.A., Hung J., Maron M.S., Ommen S.R., Woo A., American Society of Echocardiography, American Society of Nuclear Cardiology, Society for Cardiovascular Magnetic Resonance, & Society of Cardiovascular Computed Tomography. 2011. American Society of Echocardiography clinical recommendations for multimodality cardiovascular imaging of patients with hypertrophic cardiomyopathy: Endorsed by the American Society of Nuclear Cardiology, Society for Cardiovascular Magnetic Resonance, and Society of Cardiovascular Computed Tomography. Journal of the American Society of Echocardiography: official publication of the American Society of Echocardiography, 24(5), 473–498. doi: 10.1016/j.echo.2011.03.006
Nagueh S.F., Smiseth O.A., Appleton C.P., Byrd 3rd B.F., Dokainish H., Edvardsen T., Flachskampf F.A., Gillebert T.C., Klein A.L., Lancellotti P., Marino P., Oh J.K., Popescu B.A., Waggoner A.D. 2016. Recommendations for the evaluation of left ventricular diastolic function by echocardiography: An update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. J. Am. Soc. Echocardiogr., 29(4): 277–314. doi: 10.1016/j.echo.2016.01.011.
Nagueh S.F., Phelan D., Abraham T., Armour A., Desai M.Y., Dragulescu A., Gilliland Y., Lester S.J., Maldonado Y., Mohiddin S., Nieman K., Sperry B.W., Woo A. 2022. Recommendations for multimodality cardiovascular imaging of patients with hypertrophic cardiomyopathy: an update from the American Society of Echocardiography, in Collaboration with the American Society of Nuclear Cardiology, the Society for Cardiovascular Magnetic Resonance, and the Society of Cardiovascular Computed Tomography. Journal of the American Society of Echocardiography: official publication of the American Society of Echocardiography, 35(6), 533–569. doi: 10.1016/j.echo.2022.03.012
Nie C., Zhu C., Xiao M., Yang Q., Meng Y., Wu R., Wang S. 2021. Mid-ventricular obstruction is associated with non-sustained ventricular tachycardia in patients with hypertrophic obstructive cardiomyopathy. Clin Cardiol, 44(4): 555–562. doi: 10.1002/clc.23575
Oliveira D.C., Assunção F.B., Santos A.A., Nacif M.S. 2016. Cardiac magnetic resonance and computed tomography in hypertrophic cardiomyopathy: an update. Arquivos brasileiros de cardiologia, 107(2), 163–172. doi: 10.5935/abc.20160081
Ommen S.R., Mital S., Burke M.A., Day S.M., Deswal A., Elliott P., Evanovich L.L., Hung J., Joglar J.A., Kantor P., Kimmelstiel C., Kittleson M., Link M.S., Maron M.S., Martinez M.W., Miyake C.Y., Schaff H.V., Semsarian C., Sorajja P. 2020. 2020 AHA/ACC guideline for the diagnosis and treatment of patients with hypertrophic cardiomyopathy: executive summary: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Journal of the American College of Cardiology, 76(25), 3022–3055. doi: 10.1016/j.jacc.2020.08.044
Panetta D., Gabelloni M., Faggioni L., Pelosi G., Aringhieri G., Caramella D., Salvadori P.A. 2021. Cardiac computed tomography perfusion: contrast agents, challenges and emerging methodologies from preclinical research to the clinics. Academic radiology, 28(1), e1–e13. doi:10.1016/j.acra.2019.12.026
Quarta G., Aquaro G.D., Pedrotti P., Pontone G., Dellegrottaglie S., Iacovoni A., Brambilla P., Pradella S., Todiere G., Rigo F., Bucciarelli-Ducci C., Limongelli G., Roghi A., Olivotto I. 2018. Cardiovascular magnetic resonance imaging in hypertrophic cardiomyopathy: the importance of clinical context. Eur. Heart. J. Cardiovasc. Imaging, 19(6): 601–610. doi: 10.1093/ehjci/jex323
Rashdan L., Hodovan J., Masri A. 2023. Imaging cardiac hypertrophy in hypertrophic cardiomyopathy and its differential diagnosis. Current opinion in cardiology, 38(5), 397–404. doi: 10.1097/HCO.0000000000001070
Robich M.P., Schaff H.V., Ortoleva J., Patlolla S.H., Zaky M.H., Cobey F.C., Chen F.Y. 2023. Understanding septal morphology in hypertrophic cardiomyopathy-implications for the surgeon. The Journal of thoracic and cardiovascular surgery, 166(2), 514–518. doi: 10.1016/j.jtcvs.2022.09.059
Rowin E.J., Maron B.J., Olivotto I., Maron M.S. 2017. Role of exercise testing in hypertrophic cardiomyopathy. JACC. Cardiovascular imaging, 10(11), 1374–1386. doi: 10.1016/j.jcmg.2017.07.016
Sakellaropoulos S., Svab S., Mohammed M., Dimitra L., Mitsis A. 2021. The role of mitral valve in hypertrophic obstructive cardiomyopathy: An Updated Review. Current problems in cardiology, 46(3), 100641. doi: 10.1016/j.cpcardiol.2020.100641
Sherrid M.V., Adams D.H. 2020. The mitral valve in hypertrophic cardiomyopathy: other side of the outflow tract. Journal of the American College of Cardiology, 76(19), 2248–2251. doi: 10.1016/j.jacc.2020.09.580
Stewart M., Elagizi A., Gilliland Y.E. 2023. Imaging of left ventricular outflow tract obstruction in hypertrophic cardiomyopathy. Current opinion in cardiology, 38(5), 405–414. doi: 10.1097/HCO.0000000000001058
Tower-Rader A., Kramer C.M., Neubauer S., Nagueh S.F., Desai, M.Y. 2020. Multimodality imaging in hypertrophic cardiomyopathy for risk stratification. Circulation. Cardiovascular imaging, 13(2), e009026. doi: 10.1161/CIRCIMAGING.119.009026
Turvey L., Augustine D.X., Robinson S., Oxborough D., Stout M., Smith N., Harkness A., Williams L., Steeds R.P., Bradlow W. 2021. Transthoracic echocardiography of hypertrophic cardiomyopathy in adults: a practical guideline from the British Society of Echocardiography. Echo research and practice, 8(1), G61–G86. doi: 10.1530/ERP-20-0042
Urbano-Moral J.A., Rowin E.J., Maron M.S., Crean A., Pandian N.G. 2014. Investigation of global and regional myocardial mechanics with 3-dimensional speckle tracking echocardiography and relations to hypertrophy and fibrosis in hypertrophic cardiomyopathy. Circ. Cardiovasc. Imaging, 7(1): 11–19. doi: 10.1161/CIRCIMAGING.113.000842
Weissler-Snir A., Crean A., Rakowski H. 2016. The role of imaging in the diagnosis and management of hypertrophic cardiomyopathy. Expert review of cardiovascular therapy, 14(1), 51–74. doi: 10.1586/14779072.2016.1113130
Wengrofsky P., Akivis Y., Bukharovich I. 2023. Cardiac multimodality imaging in hypertrophic cardiomyopathy: what to look for and when to image. Current cardiology reviews, 19(5), 1–18. doi: 10.2174/1573403X19666230316103117
Williams L.K., Frenneaux M.P., Steeds R.P. 2009. Echocardiography in hypertrophic cardiomyopathy diagnosis, prognosis, and role in management. European Journal of Echocardiography, 10(8), III9–III14. doi:10.1093/ejechocard/jep157
Zemanek D., Tomasov P., Bělehrad M., Hladká K., Košťálová J., Kára T., Veselka J. 2015. Comparison of sublingual isosorbide dinitrate and Valsalva maneuver for detection of obstruction in hypertrophic cardiomyopathy. Arch. Med. Sci., 11(4): 751–755. doi: 10.5114/aoms.2015.47096